1 413
������������⣺(1)д��������Ӧ�Ļ�ѧ����ʽ��?
(2)�����������ݣ�����һ�·�Ӧ�����˵��¶��� ��(����)?
A������770 ��
B��850 ��?
C������882.9 ��
D��1423~1500 ��
�ο��𰸣�(1)Na+KCl ������������Ǹ��ݼء����۷е�IJ����������ѧ��Ӧ��������ӡ�����������״̬�·��������ӱ任�ķ�Ӧ�����������شﵽ�е㣬���������ʴﵽ�ۻ�״̬����Ӧ�ŵ���ʵ�֡������¶�ѡ���ڸ���770 �������882.9 �档 ������������Ǹ��ݼء����۷е�IJ����������ѧ��Ӧ��������ӡ�����������״̬�·��������ӱ任�ķ�Ӧ�����������شﵽ�е㣬���������ʴﵽ�ۻ�״̬����Ӧ�ŵ���ʵ�֡������¶�ѡ���ڸ���770 �������882.9 �档
�����Ѷȣ���
2�������� ��13�֣���10gCO2��CO�Ļ����ͨ��װ������Na2O2�ĸ���ܣ���Ӧ�����ܵ�������������5.6g����ԭ���������CO2����������Ϊ���٣�
�ο��𰸣�88%.
���������������ģ�������Ӧ�Ļ�ѧ����ʽΪ��
2CO2��2Na2O 2===2Na2CO3��O2?????�Sm?????????????????? ..............3�� 2===2Na2CO3��O2?????�Sm?????????????????? ..............3��
2��44g???????????????????????? 56g
m��CO2��?????????????????????
�����Ѷȣ�һ��
3��ѡ���� ��ͼģ�⡰�����Ƽ����ȡNaHCO3�IJ���װ�á����в�����ȷ����
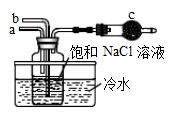
A��aͨ��CO2��Ȼ��bͨ��NH3��c�зż�ʯ��
B��bͨ��NH3��Ȼ��aͨ��CO2��c�зż�ʯ��
C��aͨ��NH3��Ȼ��bͨ��CO2��c�з�պϡ�������֬��
D��bͨ��CO2��Ȼ��aͨ��NH3��c�з�պϡ�������֬��
�ο��𰸣�C
���������
�������������CO2��ˮ�е��ܽ��С����������������ˮ�������ͨ�백����Ȼ����ͨ��CO2�����ڰ�����������ˮ��Ҫ��ֹ���������aͨ��NH3��bͨ��CO2�������Ǽ���������Ҫϡ�������ն���İ�������ѡC��
�����Ѷȣ���
4��ʵ���� ��ѧ��һ����ʵ��Ϊ��������Ȼ��ѧ����������ʵ��֪ʶ�ش��������⡣
��1������˵�������??????????????��?
A����Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ���
B����Cl2ͨ����ɫʯ����Һ����Һ�ȱ�����ɫ
C������1L0.5mol��L-1��NaCl��Һ������������ӳ���29.25gNaCl����
D�������£�������������������Ũ����
E��ʵ���ұ�������������Һ�������Լ�ƿ�ڼ������ۻ���������ֹ��������������
F��ʵ���ҿ����ü����Ȼ�淋ķ�����ȡ��������
��2����֪ij���������к���NaCl���ʣ�Ϊ�ⶨ�����д��������������������ͼ��ʾ��װ�ý���ʵ�顣ʵ���������ӵ���a����������һ�����Ŀ�����

��װ��E������?????????????���Լ�bΪ??????????????????��
��ʵ���������Ҫ�ⶨ�����ݳ���Ʒ�������У�????????????������ţ���
A.��Ӧǰ��װ��C������????? B.��Ӧǰ��װ��D������?????? C.��Ӧǰ��װ��E������
����ȥ��װ��A����ⶨ���?????????(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��
�ο��𰸣���1��C F??��2���ٸ����??��ʯ��??�� B?????
���������
�����������1��A���Ϸ�Һ©����Һ��ų��Ĺ�����ȷ��B. Cl2����ˮ������Ӧ��Cl2��H2O HCl��HClO��������HCl��HClO�����ᣬ��ʹ��ɫʯ����Һ��Ϊ��ɫ��������HClO��ǿ�������ԣ��ֻ�Ѻ�ɫ��������ɫ���ʽ�Cl2ͨ����ɫʯ����Һ����Һ�ȱ�����ɫ����ȷ��C.������ӵ�ȷ��Ϊ0.1g, HCl��HClO��������HCl��HClO�����ᣬ��ʹ��ɫʯ����Һ��Ϊ��ɫ��������HClO��ǿ�������ԣ��ֻ�Ѻ�ɫ��������ɫ���ʽ�Cl2ͨ����ɫʯ����Һ����Һ�ȱ�����ɫ����ȷ��C.������ӵ�ȷ��Ϊ0.1g,
�����Ѷȣ�һ��
5��ѡ���� �ѵ��������ƽ�������ʵ�飬������������������
A�����Ʒ�������ϡ������
B�����Ʒ�������ˮ��
C�����Ʒ�������ͭ��Һ��
D���������������ò���ЩС�ף��ٷ���ˮ��
�ο��𰸣�D
���������������������Ͷ�뵽ˮ��ϡ���ᡢϡ�����У������Ʋμӵķ�Ӧ�����Էų�������������ȣ�
�������������ò���һЩС�ף��ٷ���������ˮ�У�����������ˮ��Ӧ����NaOH����������������Ľ�����������ǿ�ᷴӦҲ����ǿ�Ӧ������������������NaOH��Һ��ӦҲ������������D������������࣮
��ѡD��
���������⿼���ƵĻ�ѧ���ʣ��ѶȲ���ע�����������ᷴӦ������Ӧ�����ʣ��������������ͭ��Һ��Ӧ����
�����Ѷȣ�һ��
|