微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________, K值大小与温度的关系是:温度升高,K值______________ (填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)
 CO2(g)十H2(g)十Q(Q>0) CO和H2O浓度变化如下图,则0-4min的平均反应速率v(CO)=______
CO2(g)十H2(g)十Q(Q>0) CO和H2O浓度变化如下图,则0-4min的平均反应速率v(CO)=______
mol/(L・min)
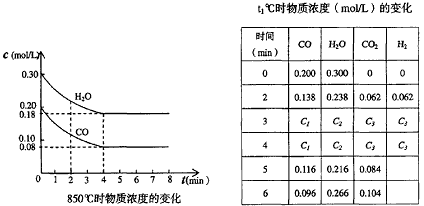
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min-4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min-5min问,平衡向逆方向移动,可能的原因是________(单选),表中5min-6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
参考答案:(1)可逆反应的进行程度越大;可能增大也可能减小
(2
本题解析:
本题难度:一般
2、选择题 下列说法中,不正确的是 [???? ]
A.加入适当催化剂可以改变化学反应速率,但不可提高反应物的转化率
B.放热反应的反应速率一定比吸热反应的反应速率大
C.相同条件下,等体积的H2和空气含有相同数目的分子
D.常温常压下,1molN2和28gCO含有相同的原子数
参考答案:A
本题解析:
本题难度:一般
3、填空题 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为: C(s)+H2O(g)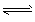 CO(g)+H2 (g) △H =+131. 3kJ・mol-1 一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是____(填字母,下同)。
CO(g)+H2 (g) △H =+131. 3kJ・mol-1 一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是____(填字母,下同)。
A.容器中的压强不变
B.1mol H-H键断裂的同时断裂2mol H-O键
C.v正(CO) =v逆(H2O)
D.c(CO) =c(H2)
在该温度下,该反应的平衡常数表达式为K=____。
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)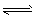 CO2 (g)+H2 (g),得到如下三组数据:
CO2 (g)+H2 (g),得到如下三组数据:
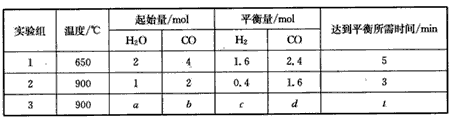
①实验1中以v(CO2)表示的反应速率为____。
②该反应为____(填“吸”或“放”)热反应。
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是___(用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+ 3H2 (g) CH3OH(g)+H2O(g),下图表示该反应进行过程中能量(单位为 kJ・mol-1)的变化。在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c(CH3OH)增大的是 (? ?)
CH3OH(g)+H2O(g),下图表示该反应进行过程中能量(单位为 kJ・mol-1)的变化。在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c(CH3OH)增大的是 (? ?)
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来
D.再充入1mol CO2和3mol H2

参考答案:(1)B、C;![]() 本题解析:
本题解析:
本题难度:一般
4、选择题 关节炎的病因主要是在关节滑液中形成了尿酸钠晶体,主要反应为:Ur-+Na+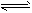 NaUr(s);第一次关节炎发作往往在冬季,有关该反应的说法中,正确的是 [???? ]
NaUr(s);第一次关节炎发作往往在冬季,有关该反应的说法中,正确的是 [???? ]
A.正反应是吸热反应
B.正反应是放热反应
C.升高温度平衡向正反应方向移动
D.以上说法都不正确
参考答案:B
本题解析:
本题难度:一般
5、填空题 一定条件下,将SO2和O2充入一个体积为2L的密闭容器中,发生如下反应:2SO2(g)+O2(g)
 2SO3(g),反应过程中SO2、O2、SO3物质的量变化如图所示。
2SO3(g),反应过程中SO2、O2、SO3物质的量变化如图所示。
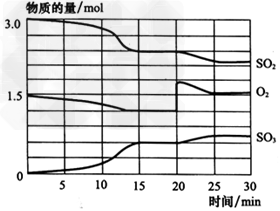
回答下列问题:
(1)0~15min内SO2的平均反应速率为__________。
(2)当降低温度时,SO2的转化率增大,则该反应正反应为_________(填“吸热”或“放热”)反应。
(3)若反应达到平衡后,其他条件不变,向该容器中充入2mol SO2气体,则平衡常数K____(填“增大”“减小”或“不变”)。
(4)反应处于平衡状态的时间是____,则该温度下的平衡常数K为____(保留2位小数);若t℃时平衡常数为K1,(t+50)℃时平衡常数为K2,则K1____(填“>” “<”或“=”)K2。
(5)反应进行至20min时,曲线发生变化的原因是 _____________(用文字表达);10~15min的曲线变化的原因可能是_____(填写编号)。
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量
(6)某温度下的平衡常数K=532.4,各物质的浓度如下,c(SO2)=0.0600mol/L,c(O2)=0.4000mol/L, c(SO3)=2.000mol/L,请判断反应进行的方向:________。
参考答案:(1)0.02mol/(L・min)
(2)放热
本题解析:
本题难度:一般