微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物酸锰(MnFe2O4)也可用于热化学循环分解水制氢,MnFe2O4的制备流程如下:
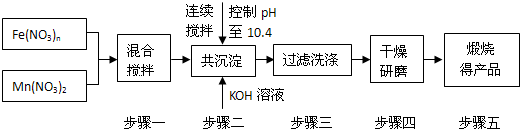
(1)原料Fe(NO3)n中n=______,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为______.
(2)步骤二中“连续搅拌”的目的是______;步骤三中洗涤干净的标准是______.
(3)利用MnFe2O4热化学循环制氢的反应可表示为:MnFe2O4
>1000K
MnFe2O4-x+x
2
O2↑????MnFe2O4-x+xH2O→MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中X=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为______.
②该热化学循环制氢的优点有(答两点即可)______.
参考答案:(1)Mn为+2价,令MnFe2O4中Fe的化合价为a价,根
本题解析:
本题难度:一般
2、选择题 为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是(???)
A.氢氧化钠是否 变质(BaC12) 变质(BaC12)
B.FeSO4是否被氧化(KSCN)
C.KI是否被氧化(淀粉溶液)
D.K2SO3是否被氧化(BaC12)
参考答案:D
本题解析:略
本题难度:简单
3、填空题 (7分)现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
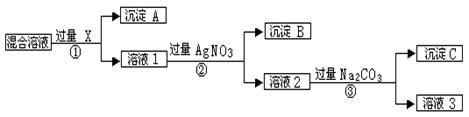
请回答下列问题:
⑴写出实验流程中下列物质的化学式
试剂X :????????????沉淀A:????????????沉淀B:?????????
⑵上述实验流程中加入过量的Na2CO3的目的是????????????????????。
⑶按此实验方案得到的溶液3中肯定含有?????????(填化学式)杂质。
参考答案:(7分)⑴BaCl2 [或Ba(NO3)2]??? BaSO
本题解析:(1)根据步骤②可知,B是氯化银,所以步骤①中的试剂是氯化钡,则A是硫酸
钡。
(2)溶液2中含有Ag+和Ba2+,所以碳酸钠的作用是除去溶液中的Ag+和Ba2+。
(3)碳酸钠是过量的,所以溶液3中一定含有碳酸钠。
本题难度:一般
4、选择题 分离菜籽油与水混合物的实验方法是[???? ]
A.过滤
B.蒸馏
C.分液
D.萃取
参考答案:C
本题解析:
本题难度:简单
5、简答题 对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、渗析、加热分解等.下列各组混合物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用______的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒.
(2)提取碘水中的碘,用______方法.
(3)除去食盐溶液中的水,可采用______的方法.
(4)海水淡化,一般采用______的方法.
(5)除去氧化钙中的碳酸钙可用______的方法.
(6)除去淀粉中的食盐可用______的方法.
参考答案:(1)可用过滤的方法除去Ca(OH)2溶液中悬浮的CaCO3
本题解析:
本题难度:一般
|