微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (16分)某化学兴趣小组欲设计使用如下装置验证:铜和一定量的浓硝酸反应有一氧化氮产生。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)
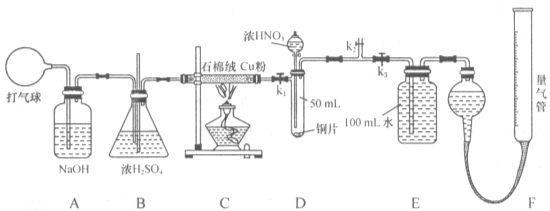
试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是________________________________;
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体是__???_(填化学式),通入该气体的目的是____________________????????; 进行此步操作时应关闭_________,打开_________ (填k1、k2或k3);
进行此步操作时应关闭_________,打开_________ (填k1、k2或k3);
(3)若C装置的硬质玻璃管中出现堵塞,则B中可能出现的现象是___________________??;
(4)关闭k1、k2,打开k3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:_________???;
(5)若E中出现倒吸,可采取的应急操作是_________________________??;
(6)从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol/L的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应______ (填“有”或“无”)NO生成。
参考答案:(1)增大铜粉与氧气的接触面积,使反应迅速、充分
(2
本题解析:本实验目的是证明铜和一定量的浓硝酸反应有一氧化氮产生,而NO与氧气不能共存,故本实验的关键之一就是保证实验装置内无氧气
(1)为了增大铜粉与氧气的接触面积,保证反应迅速充分的进行
(2)从实验装置可看出,空气经NaOH溶液吸收CO2后,再经浓硫酸干燥吸水、铜粉除去氧气,最终进入D中的气体为氮气
EF装置中已经全部充满水,故只需要将E左边的一系列装置内的空气排出即可,故关闭k3,打开k1、k2
(3)C装置的硬质玻璃管中出现堵塞,则B锥形瓶内压强增大,玻璃管内液面将上升
(4)
本题难度:一般
2、实验题 为了测定硫酸铵和氯化铵混合物中氯化铵的质量分数,甲、乙两位同学按下列实验步骤进行实验:称量样品→溶解→加过量试剂A→过滤出现沉淀B→洗涤沉淀→烘干称量→处理实验数据并得出结果。
(1)实验时,甲同学选用硝酸银溶液作试剂A,乙同学选用氯化钡溶液作试剂A,其中同学所选的试剂A不合理,理由是________________。
(2)以下都是在试剂A选择正确时进行的实验:
①为进行称量、溶解、反应、过滤、洗涤沉淀的各项操作,准备了以下仪器:托盘天平与砝码,烧杯、过滤器、铁架台及附件,胶头滴管、量筒,其中还缺少一件必备的仪器是_____________。
②若过滤所得沉淀未经洗涤烘干称量,测得结果将________(填“偏高”或“偏低”)。
③若实验测得混合物的质量为W g,沉淀物的质量为m g,实验测定的氯化铵质量分数计算式=_____________。
参考答案:(1)甲因为AgNO3既可以与NH4Cl反应生成AgCl白色
本题解析:(1)甲同学选用试剂A是错的,因为AgNO3既可以与NH4Cl反应生成AgCl白色沉淀,又可与(NH4)2SO4反应生成微溶于水的Ag2SO4,达不到实验目的。
(2)①玻璃棒,溶解、洗涤、过滤等各步均需使用玻璃棒。
②未经洗涤、烘干就称量,使得称量数值比实际数值大,造成求出的NH4Cl质量分数偏低。
③(NH4)2SO4+BaCl2====BaSO4↓+2NH4Cl
132??????????????? 233
x?????????????????m g
x=
本题难度:简单
3、选择题 在标准状况下,1 L水中溶解700 L NH3,所得溶液的密度为0.9 g・cm-3,则氨水的浓度为
A.18.4 mol・L-1
B.20.4 mol・L-1
C.37.7%
D.38.5%
参考答案:A
本题解析:1 L水中溶解700 L NH3的物质的量为700 L/22.4 L・mol-1="700/22.4" mol="31.3" mol,溶液的体积为:
(1 000 g+700/22.4 mol×17 g・mol-1)÷900 g・L-1="1.7" L
物质的量浓度为31.3 mol÷1.7 L="18.4" mol・L-1。
本题难度:简单
4、选择题 室温时,容量为18 mL的试管里充满NO2气体,然后将它倒置于水中,直到管内水面不再上升为止,再通入6 mL O2,最后试管内还有( )?
A.3 mL O2
B.1.5 mL O2?
C.3 mL NO
D.1.5 mL NO?
参考答案:B?
本题解析:18 mL NO2溶于水3NO2~NO,可产生NO为6 mL,再通入6 mL? O2,发生4NO+3O2+2H2O4HNO3,43="6" mLn(O2),n(O2)="4.5" mL,所以余n(O2)="6" mL-4.5 mL="1.5" mL,答案?为B。
本题难度:简单
5、选择题 由红磷制取白磷可采用的方法是????????????????????????(???)???????
A.在空气中加热至416℃,使红磷升华
B.用CS2溶解,将红磷分出
C.加高温、高压,使红磷分出
D.隔绝空气,加热到416℃,使红磷升华,再冷却
参考答案:D 本题解析:红磷与白磷的区别。白磷白色蜡状不溶于水,溶于CS2 剧毒着火点40℃ , 易自燃密封,保存于冷水。红磷红棕色粉末不溶于水和CS2 无毒 着火点240℃密封,防止吸湿。
本题解析:红磷与白磷的区别。白磷白色蜡状不溶于水,溶于CS2 剧毒着火点40℃ , 易自燃密封,保存于冷水。红磷红棕色粉末不溶于水和CS2 无毒 着火点240℃密封,防止吸湿。
本题难度:简单