微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质不能与氢氧化钠溶液反应的是( )
A.Fe2O3
B.Al(OH)3
C.NaHCO3
D.H2SiO3
参考答案:A
本题解析:
本题难度:简单
2、填空题 粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物,现进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.2 L 6.0 mol / L的盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出标准状况下4.48L的气体,生成溶液D,同时还有残留的单质B。请你填写下列空白:
(1)①中铝热反应的化学方程式是_____________,产物中单质B的化学式是___________。
(2)③中反应的离子方程式是____________、____________。
(3)20g A中n(Fe2O3)=_________;若溶液D的体积仍视为0.2L ,则该溶液中c(Mg2+)=_______,c(Fe2+)=_______。
参考答案:(1)2Al+Fe2O3![]() 本题解析:
本题解析:
本题难度:一般
3、填空题 (4分)有人在研究硫酸亚铁(FeSO4)受热分解时,作出了两种假设:
(1)假设它按KClO3受热分解的方式分解,反应的化学方程式为?????????????????????;
(2)假设它按CaCO3受热分解的方式分解,反应的化学方程式为??????????????????????;
参考答案: 本题解析:略
本题解析:略
本题难度:一般
4、选择题 在Fe2(SO4)3溶液中,加入ag?Cu,完全溶解后,又加入bg?Fe,充分反应后得到cg?残余固体,且a>c,则下列判断不正确的是( )
A.最后溶液中一定不含Fe3+
B.残余固体可能是Fe、Cu的混合物
C.最后溶液中一定含Fe2+
D.残余固体一定是Cu
参考答案:此题中发生的化学反应有三个,方程式如下:2FeCl3+Cu=
本题解析:
本题难度:一般
5、填空题 (14分)利用废铁丝、硫酸铜废液(含硫酸亚铁)和被有机物污染的废铜粉制备硫酸铜晶体。生产过程如下:

试回答下列问题:
(1)铁丝在投入硫酸铜废液前需用稀H2SO4进行处理,可能发生反应的离子方程式有?????????????。
(2)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)?????????????????。
在实验室中,常将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示)。
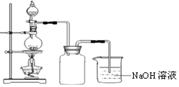
(3)写出烧瓶中发生反应的离子方程式为????????????????????????????????
(4)广口瓶的作用是?????????????????
(5)为符合绿色化学的要求,某研究性学习小组进行如下
设计:将3.2 g铜丝放到45 mL 1.5 mol・L-1的稀硫酸中,控温在50 ℃。加入18 mL 10%的H2O2,反应0.5h后,升温到60 ℃,持续反应1 h后,过滤、蒸发浓缩、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4・5H2O 10.5 g。请回答:
①加热时温度不宜过高的原因是???????????????????????????;
②本实验CuSO4・5H2O的产率为??????????????。
参考答案:⑴? Fe2O3+6H+=2Fe3++3H2O,2Fe3++
本题解析:
试题分析:(1)铁丝表面有铁锈。投入稀H2SO4中发生反应的两种方程式为:Fe2O3+6H+=2Fe3++3H2O;2Fe3++Fe=3Fe2+;Fe+2H+=Fe2++H2↑;(2)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是使Cu变为氧化铜,与酸反应得到CuSO4.反应的方程式为:2Cu+O2+2H2SO4=2CuSO4+2H2O 或2Cu+O2=2CuO,CuO+H2SO4=CuSO4+H2O ;(3)在烧瓶中Cu与稀硝酸发生反应的离子方程式为:
本题难度:一般