微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列化合物分子,在核磁共振氢谱图中能给出三种信号峰的是
[???? ]
A.CH3CH2CH3
B.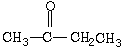
C.CH3-O-CH3
D.
参考答案:B
本题解析:
本题难度:一般
2、填空题 没有支链的化合物A的分子式为C5H8O2,A可以使Br2的四氯化碳溶液褪色,经红外光谱分析,A分子中含有-COOH(已知-COOH不能使Br2的四氯化碳溶液褪色),则A可能的结构简式为:___________,
__________,____________。
参考答案:CH2=CHCH2CH2COOH;CH3CH=CHCH2CO
本题解析:
本题难度:一般
3、选择题 化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱见图1和图2。关于A的下列说法正确的是
 [???? ]
[???? ]
A. A分子属于酯类化合物,在一定条件下能发生水解反应
B.1molA在一定条件下可与4 mol H2发生加成反应
C.符合题中A分子结构特征的有机物只有一种
D.与A属于同类化合物的同分异构体只有2种
参考答案:AC
本题解析:
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值,下列说法正确的是
A.在标准状况下,VL水含有的氧原子个数为NA
B.常温下,2L1mol?L-1的乙酸溶液中,所含分子总数小于2NA
C.1molFeCl3跟水完全反应转化为氢氧化铁胶制后,其中胶体粒子的数目为NA
D.1molNH2-中含电子数为10NA
参考答案:D
本题解析:分析:A、标准状况下,水为液体,Vm≠22.4L/mol;
B、乙酸溶液中除了含有乙酸分子外,还含有水分子;
C、氢氧化铁胶体粒子为若干个“Fe(OH)3”的集合体;
D、根据组成原子的结构和电荷分析.
解答:A、标准状况下,水为液体,Vm≠22.4L/mol,不能用气体的气体摩尔体积计算,故A错误;
B、乙酸溶液中除了含有乙酸分子外,还含有水分子,则2L1mol?L-1的乙酸溶液中,所含分子总数远大于2NA,故B错误;
C、氢氧化铁胶体粒子为若干个“Fe(OH)3”的集合体,则胶体粒子的数目小于NA,故C错误;
D、1molNH2-中含电子数为(7+2+1)mol×NA/mol=10NA,故D正确.
故选D.
点评:本题考查阿伏加德罗常数,题目难度不大,注意物质的组成、结构、性质和存在条件是否标准状态以及物质的聚集状态等问题,解答此类题目时,常从以上几个角度考虑.
本题难度:简单
5、选择题 下列各组物质中,所含有的分子数相同的是
A.10gH2和10gO2
B.9gH2O和0.5molBr2
C.5.6L?N2和11gCO2
D.224mLH2(标准状况)和0.1mol?N2
参考答案:B
本题解析:分析:A.根据n= 计算各物质的物质的量;
计算各物质的物质的量;
B.根据n= 计算?H2O的物质的量;
计算?H2O的物质的量;
C.氮气不一在标况的条件,根据n= 计算CO2的物质的量;
计算CO2的物质的量;
D.根据n= 计算H2的物质的量;
计算H2的物质的量;
解答:A.10gH2的物质的量为n= =
= =5mol,10gO2的物质的量为n=
=5mol,10gO2的物质的量为n= =
=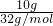 =
= mol,二者物质的量不相等,所含分子数不相等,故A错误;
mol,二者物质的量不相等,所含分子数不相等,故A错误;
B.H2O的物质的量为n= =
= =0.5mol,0.5?mol?Br2,则二者的物质的量相同、分子数相同,故B正确;
=0.5mol,0.5?mol?Br2,则二者的物质的量相同、分子数相同,故B正确;
C.在标准状况下,Vm=22.4L/mol,CO2的物质的量为n= =
= =0.5mol,5.6L氮气的存在条件不一定是标况,它的物质的量不清楚,则二者的物质的量不同,即所含分子数不同,故C错误;
=0.5mol,5.6L氮气的存在条件不一定是标况,它的物质的量不清楚,则二者的物质的量不同,即所含分子数不同,故C错误;
D.在标准状况下,Vm=22.4L/mol,224mL=0.224L,则H2的物质的量为n= =
= =0.01mol,而N2的物质的量为0.1mol,则二者的物质的量不同,即所含分子数不同,故D错误;
=0.01mol,而N2的物质的量为0.1mol,则二者的物质的量不同,即所含分子数不同,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的有关问题,注意物质与微粒的关系,注意单位的运用,题目较简单.
本题难度:简单