��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (8��)̼���ƺ�̼�������������г��������ʡ���ش��������⡣
��1��̼���ƵĻ�ѧʽ��?????????���׳�???????����ˮ��Һ��????�ԣ���ᡱ��������С���, ����ɫ��Ӧ�г�______ɫ��̼���Ƶ��׳�_________��
��2�������ʵ�����̼���ƺ�̼���������������ᷴӦ����CO2������ǰ��?????���ߣ����������д�������ᷴӦ�����ӷ���ʽ????????????????????????????
��3��д��̼���������� �ֽ�Ļ�ѧ����ʽ��???????????????????????????
�ο��𰸣���1��NaHCO3??С�մ�??��??�մ���ߴ��� ��2��C
���������
�����������1��̼�����ƣ���ѧʽΪNaHCO3���׳�С�մ���ˮ��Һ����̼�������Ҫ����ˮ�⣬ʹ����Һ�ʼ��ԡ�̼���Ƶ��׳��մ���ߴ��
��2��NaHCO3��HCl��Ӧ�Ļ�ѧ����ʽΪ��NaHCO3+HCl=NaCl+H2O+CO2����Na2CO3��HCl��Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+2HCl=2NaCl+H2O+CO2����������������ѧ����ʽ���Կ����������ʵ�����Na2CO3��NaHCO3�ֱ���HCl��Ӧ������CO2�����ʵ���֮��Ϊ1��1��
��3��̼���������ȷֽ����Ϊ��̼���ơ�ˮ
�����Ѷȣ�һ��
2������� ��Ԫ�����Ƿֲ�����ģ�25ʱ̼��Ͳ����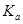 ���±���
���±���
H2CO3
| Ka1=4.3��10-7
| H2C2O4
| Ka1=5.6��10-2
|
Ka2=5.6��10-11
| Ka2=5.42��10-5
?
��1����������������Һ��
A��0.1 mol/L��Na2C2O4��Һ??????? B��0.1 mol/L��NaHC2O4��Һ
C��0.1 mol/L��Na2CO3��Һ???????? D��0.1 mol/L��NaHCO3��Һ
����c(H��)������_________��c��OH����������_________ ��
��2��ij��ѧʵ����ȤС��ͬѧ���ô���ʯ��ϡ�����Ʊ�CO2�����Һ�еμ�̼������Һ������Һ�в���pH�����������pH�仯������ͼ��ʾ��
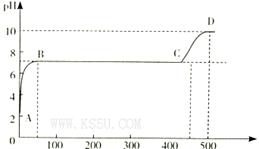
�տ�ʼ����̼������Һʱ������Ӧ�����ӷ���ʽΪ_________��BC�η�����Ӧ�����ӷ���ʽΪ_____��D��ʱ�����Һ����ˮ���������c��H+��="_________" mol/L��
�ο��𰸣���1��B ??C??��2��2H++CO32-=H2O+CO2
���������
�����������1����ΪH2C2O4�Ķ�������ƽ�ⳣ��Ka2=5.42��10-5> H2CO3�Ķ�������ƽ�ⳣ��Ka2=5.6��10-11����������������Һc(H��)������0.1 mol/L��NaHC2O4��Һ����ȷѡ��ΪB������ƽ�ⳣ��ԽС��������ˮ��ij̶Ⱦ�Խ����Һ�ļ��Ծ�Խǿ������Ka2(H2C2O4)=5.42��10-5> 5.6��10-11= Ka2(H2CO3),����c��OH����������0.1 mol/L��Na2CO3��Һ����ȷѡ��ΪC����2���ڷ�Ӧ��ʼʱ������Һ��pH�Դ�
�����Ѷȣ�һ��
3��ѡ���� NaH��һ�����ӻ������ˮ��Ӧʱ�����ռ����������Ҳ�ܺ��Ҵ��ȷ�Ӧ�������������й���NaH����������ȷ����??????????��???��
A����ˮ��Ӧʱ��ˮ��������
B��LiH�������Ӱ뾶С�������Ӱ뾶
C�����Ҵ���Ӧʱ���ų��������ٶȱȸ�ˮ��Ӧʱ����
D����ˮ��Ӧʱ�����ɵ��ռ��ǻ�ԭ����
�ο��𰸣�A
���������NaH��H2O=NaOH��H2��
NaH��CH3CH2OH��CH3CH2ONa��H2��
A����ˮ��Ӧʱ��ˮ������������ȷ��
B��LiH�������Ӱ뾶���������Ӱ뾶��Li����H�D���Ӳ�ṹ��ͬ��Li���˵�����뾶С��
C�����Ҵ���Ӧʱ���ų��������ٶȱȸ�ˮ��Ӧʱ�������Ҵ����ǻ��ϵ����ˮ���ѵ��롣
D����ˮ��Ӧʱ�����ɵ��������ǻ�ԭ��������������
�����Ѷȣ���
4��ѡ���� ���й����Ƽ��仯�������������ȷ����
A������һ�ֻҺ�ɫ�����н��������ʵ����Ľ���
B����������������Ƶ���ɫ��ͬ
C����Ϊ�Ƶ����ʷdz����ã�����Ȼ����������̬��
D���������ƿ�����DZͧ�Ĺ�����
�ο��𰸣�A
�����������
�����Ѷȣ���
5��ѡ���� �����Ʒֱ���������Һ��Ӧʱ�������������а�ɫ�����������ǣ�
A FeCl3��Һ???? B BaCl2��Һ?????????? C MgCl2��Һ????????? D NH4Cl��Һ
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
|