��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ɫ��Fe(NO3)2��Һ����μ���ϡ����ʱ����Һ��ɫ�ı仯Ӧ���ǣ�???��
A����ɫ��dz
B������
C��û�иı�
D�����ػ�ɫ
�ο��𰸣�D
���������Fe(NO3)2��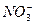 ��HCl��H+��ϳ�HNO3��Fe2+��������Fe3+��
��HCl��H+��ϳ�HNO3��Fe2+��������Fe3+��
�����Ѷȣ���
2��ѡ���� ���������У���ȷ����[???? ]
A��������Ԫ�ص�����һ�����������ӡ���
B����������ԭ��Ӧ�У��ǽ�������һ��������������
C��ijԪ�صĻ���̬��Ϊ����̬ʱ����Ԫ��һ������ԭ����
D�����������ӱ���ԭ��һ���õ���������
�ο��𰸣�D
���������������
ѡ��A��������Ԫ�ص����ӿ�����������Ҳ�����������ӣ��ʴ���
ѡ��
�����Ѷȣ���
3��ѡ���� �������ǿ�������·ֽ⣬���ɰ�����������������ˮ����Ӧ���ɵ���������ͻ�ԭ����ķ���֮���� [???? ]
A��1��3
B��2��3
C��1��1
D��4��3
�ο��𰸣�A
����������⣺�÷�Ӧ�У�NH4+��N2����Ԫ�صĻ��ϼ���-3�ۡ�0�ۣ�ʧ���ӻ��ϼ����ߣ�������ǻ�ԭ�����������������һ��笠�����ʧȥ3�����ӣ�SO42-��SO2����Ԫ�صĻ��ϼ���+6�ۡ�+4�ۣ��õ��ӻ��ϼ۽��ͣ�������������������������ǻ�ԭ���һ����������ӵõ�2�����ӣ�����С��������6������Ԫ�ظ���ԭ���غ���ƽ�÷���ʽ������ʽΪ
3��NH4��2SO4=4NH3��+3SO2��+N2��+6H2O��������������ͻ�ԭ��������ʵ���֮��=1
�����Ѷȣ���
4��ѡ���� �����з�Ӧ��2KMnO4 + 5K2SO3 + 3H2SO4 �T�T 6K2SO4 + 2MnSO4 + 3H2O ���ڷ�Ӧ�л�ԭ�����������������ʵ���֮��Ϊ[???? ]
A��1��4
B��1��3
C��2��5
D��3��2
�ο��𰸣�C
���������
���������
�ڷ�Ӧ��2KMnO4 + 5K2SO3 + 3H2
�����Ѷȣ���
5��ѡ���� ͭ��þ�ĺϽ�4.6g��ȫ����Ũ���ᣬ����Ӧ�����ᱻ��ԭֻ����4480mL��NO2�����336mlN2O4���������㵽��״�������ڷ�Ӧ�����Һ�У���������������������Һ�����ɳ���������Ϊ��??����
A��8.51g
B��8.26g
C��7.04g
D��9.02g
�ο��𰸣�A
���������
����������������֪����Ӧ�����������ۺϳ�NO2һ���ǣ�4480mL��10-3+336ml10-3��2��/22.4L��mol-1=0.23mol���г��÷�Ӧ�ķ���ʽ��Cu+HNO3=Cu(NO3)2+2NO2��+H2O, Mg+HNO3=" Mg" (NO3)2+2NO2��+H2O����Ͻ���ͭ�����ʵ���Ϊx��þ�����ʵ���Ϊy������г����̢�64g/mol��x+24g/mol��y=4.6g����2x+2y=0.23mol�����Ϣ٢ڼ��ɽ��x��y�ֱ�Ϊ0.046mol��0.069mol���������Ӧ�ij���
�����Ѷȣ���