微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+ H2O,下列各组实验中最先出现浑浊的是 [???? ]
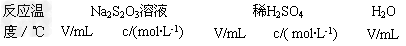
A. 25 5 0.1 10 0.1 ? ? 5
B. 25 5 0.2 5 0.2 10
C. 35 5 0.1 10 0.1 5
D. 35 5 0.2 5 0.2 10
参考答案:D
本题解析:
本题难度:一般
2、选择题 过量的两份锌粉a和b,分别加入等量的稀硫酸中,并向a中加入少量CuSO4溶液,下图表示产生H2的体积(V)与时间(t)的关系正确的是(???)????????????????????????????????????????????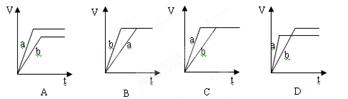
参考答案:C
本题解析:
试题分析:锌能和硫酸铜反应置换出铜,从而构成铜锌原电池,加快反应速率,即a中曲线的斜率大。由于锌是过量的,则生成的氢气是等量的,所以选项C正确,答案选C。
点评:该题是中等难度的试题,主要是考查学生灵活运用基础知识解决实际问题的能力的培养,有利于培养学生的逻辑推理能力。该题的关键是明确外界条件是如何影响反应速率的,如何结合图像灵活运用即可。
本题难度:一般
3、选择题 下列表述与示意图相符的是
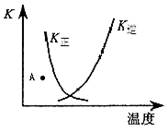
A.正反应为吸热反应
B.升高温度,有利于反应向正方向进行
C.A点时,反应向逆反应方向移动
D.K正与K逆的关系是:K正=1/K逆
参考答案:D
本题解析:
试题分析:A、根据图像可知,随着温度的升高,正方应的平衡常数逐渐减小,而逆反应的平衡常数逐渐增大,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,A不正确;B、正方应是放热反应,升高温度有利于平衡向逆反应方向移动,B不正确;C、A点在温度不变的情况下要达到平衡状态,正方应的平衡常数增大,这说明反应向正反应方向移动,即正反应速率大于逆反应速率,C不正确;D、化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此正逆反应速率的平衡常数互为倒数
本题难度:一般
4、选择题 下列有关化学反应速率的说法正确的是 [???? ]
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢
参考答案:D
本题解析:
本题难度:一般
5、选择题 反应C(s)+H2O(g)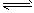 CO(g)+H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
[???? ]
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2 ④保持压强不变,充入N2
A.①④
B.①③
C.③
D.②③
参考答案:B
本题解析:
本题难度:一般