微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 化学是以实验为基础的学科。利用已学知识对下列实验进行分析并填空:
Ⅰ.(8分) 某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置完成
同主族元素非金属性强弱比较的实验研究;
乙同学设计了如图2装置实验来验证卤族元素性质的递变规律(夹持装置已略去)。A、B、C三个胶头滴管分别是氯酸钾溶液、NaBr溶液、淀粉KI溶液。已知常温下浓盐酸与氯酸钾溶液能反应生成氯气。
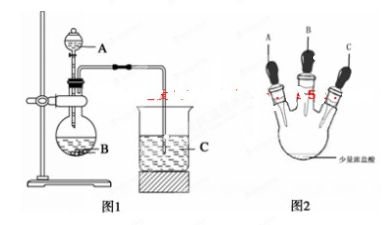
(1)甲同学设计实验所涉及的离子方程式为 、
;
(2)乙同学具体操作如下:
①先挤压胶体滴管A,使少量溶液滴入烧瓶内;
②挤压体滴管B,使稍过量溶液滴入烧瓶内,充分反应。写出该操作中主要离子方程式为 。
③再挤压体滴管C,使少量溶液滴入烧瓶内,可观察到 ;
(3)根据甲乙同学的实验可得到的结论是: 。
II.(6分) 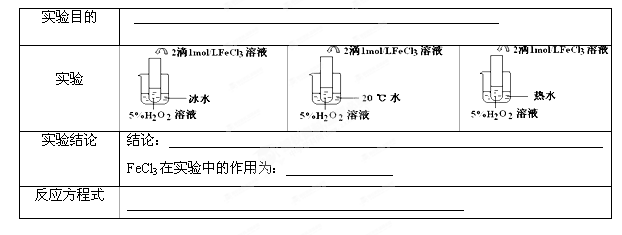
参考答案:Ⅰ(8分)(1)2H+ +CaCO3 =Ca2+ + CO2
本题解析:
试题分析:I.(1)根据元素非金属性与对应最高价含氧酸之间的关系,适合图1装置的为IVA族元素,所以甲同学设计实验所涉及的离子方程式为:2H+ +CaCO3 =Ca2+ + CO2↑ + H2O SiO32- + CO2+ H2O=H2SiO3↓ +CO32?
(2)①先挤压胶体滴管A,使少量溶液滴入烧瓶内,浓盐酸与氯酸钾溶液能反应生成氯气,②挤压体滴管B,使稍过量溶液滴入烧瓶内,氯气与NaBr溶液,离子方程式为:Cl2 + 2Br- =2Cl- +Br2
③再挤压体滴管C,使少量溶液滴入烧瓶内,Br2与KI溶液发生置换反应,生成I2,使淀粉变蓝,反应现象为:溶液颜色由黄变蓝。
(3)根据甲同学实验可得C的非金属性大于Si,根据乙同学的实验可知非金属性的强弱顺序为:Cl > Br >I,则实验结论为:同一主族,从上到下,元素非金属性减弱。
II.三组实验除温度不同外,其它条件均相同,所以实验目的为:探究温度对H2O2分解反应速率的影响;温度升高,活化分子百分率增大,所以温度越高,化学反应速率越快;FeCl3溶液在实验中的作用为:催化剂 (或加快反应速率);H2O2在FeCl3催化条件下分解,化学方程式为:2H2O2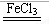 2H2O+O2 ↑。
2H2O+O2 ↑。
考点:本题考查实验方案的设计与分析、方程式的书写、实验结论的判断。
本题难度:一般
2、选择题 同时符合下列两个图象的反应是(温度T1>T2)( )
A.N2O3(g)?NO2(g)+NO(g);△H>0
B.H2(g)+I2(g)?2HI(g);△H>0
C.3NO2(g)+H2O(l)?2HNO3(l)+NO(g);△H<0
D.4NH3(g)+5O2(g)?4NO(g)+6H2O(g);△H<0
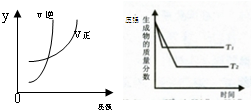
参考答案:A、可逆反应N2O3(g)?NO2(g)+NO(g)△H>0
本题解析:
本题难度:简单
3、实验题 某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72―转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4・24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
实验编号
| 初始pH
| 废水样品体积/mL
| 草酸溶液体积/mL
| 蒸馏水体积/mL
|
①
| 4
| 60
| 10
| 30
|
②
| 5
| 60
| 10
| 30
|
③
| 5
| 60
| ?
| ?
?
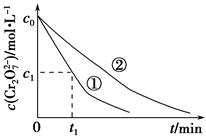
测得实验①和②溶液中的Cr2O72―浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化为________(填化学式)。
(3)实验①和②的结果表明________;实验①中0~t1时间段反应速率v(Cr3+)=________mol・L-1・min-1(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4・24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用:
假设二:________;
假设三:________;
……
(5)请你设计实验验证上述假设一,完成下表中内容。
(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4・Al2(SO4)3・24H2O、Al2(SO4)3等。溶液中Cr2O72―的浓度可用仪器测定)
实验方案(不要求写具体操作过程)
| 预期实验结果和结论
?
参考答案:(1)
实验编号
初始pH
废水样品体积/
本题解析:(1)根据题意要求,调节不同初始pH和一定浓度草酸溶液用量,做对比实验,由此可知实验③改变的是草酸溶液用量,但应保持溶液总体积不变。(2)草酸中碳的化合价为+3价,与强氧化性物质K2Cr2O7反应后,草酸应被氧化为CO2。(3)根据实验①、②的曲线对比,在相同草酸用量不同pH时,反应速率不同,所以pH对该反应有一定的影响;在0~t1时间段内,v(Cr2O72―)=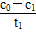
本题难度:一般
4、填空题 将除去氧化膜的镁条插入到稀盐酸溶液中,发现生成氢气的速度变化情况如图所示:
其中t1-t2?速度变化的主要原因是
______
t2-t3?速度变化的主要原因是______.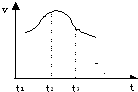
参考答案:由图可知,t1-t2?速度增大,是因该反应为放热反应,随着反
本题解析:
本题难度:一般
5、选择题 汽车尾气的无害化处理的反应为2CO(g)+2NO(g) N2(g)+2CO2(g) △H<0下列说法不正确的是 N2(g)+2CO2(g) △H<0下列说法不正确的是
A.升高温度,正逆反应速率都加快
B.使用催化剂,正逆反应速率都加快
C.使用催化剂,可以降低活化能
D.升高温度,上述反应的平衡常数会增大
参考答案:D
本题解析:反应2CO(g)+2NO(g) N2(g)+2CO2(g) △H<0正反应方向为放热反应,所以 N2(g)+2CO2(g) △H<0正反应方向为放热反应,所以
A正确,升高温度反应速率加快;B正确,催化剂能加快反应速率;C正确,催化剂能降低反应反应需的活化能,加快反应速率;D错,升高温度,该反应向逆反应方向移动,平衡常数减小;
本题难度:一般
|
|