微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 分别取40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式______.
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是______;
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃).为了计算中和热,实验时还需测量的数据有(填序号)______.
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验
序号 | 起始温度t1/℃ | 终止温度t2/℃
盐酸
氢氧化钠
混合溶液
1
20.0
20.1
23.2
2
20.2
20.4
23.4
3
20.5
20.6
23.6
依据该学生的实验数据计算,该实验测得的中和热△H=______.
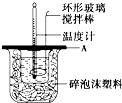
2、选择题 中和反应是典型的放热反应,酸与碱发生中和反应生成1mol水时所释放的热量称为中和热。下列关于中和热的说法正确的是[???? ]
A.中和反应生成盐和水的总能量高于酸和碱的总能量
B.稀盐酸和氢氧化钠固体反应生成1mol水释放的热量即为中和热
C.稀硫酸和氢氧化钡溶液反应生成1mol水释放的热量即为中和热
D.中和热的测定实验中应尽量防止反应中的热量损失
3、选择题 中和热测定实验中,用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验,下列说法不正确的是( )
A.改用60mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液进行反应,求出的中和热数值和原来相同
B.用50mL0.50mol/L盐酸和50mL0.55mol/LNaOH进行实验比用50mL0.50mol/L盐酸和50mL0.50mol/LNaOH测得的数值准确
C.酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌
D.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热、减少热量损失
4、选择题 下列说法正确的是( ? ) A.中和热测定实验中以环形铜丝代替环形玻璃搅拌棒会使测定值比理论值偏高
B.除去溴乙烷中溶解的溴,先用足量NaHSO3溶液洗涤,再用蒸馏水洗涤分液
C.反应N?H3(g)+HCl(g)=NH4Cl(s)△H<0在任何条件下均能自发进行
D.用标准的盐酸溶液滴定含甲基橙的氢氧化钠溶液,终点时溶液由橙色变成黄色
5、填空题 50mL?1.0mol?L-1盐酸跟50mL?1.1mol?L-1氢氧化钠溶液在图1装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
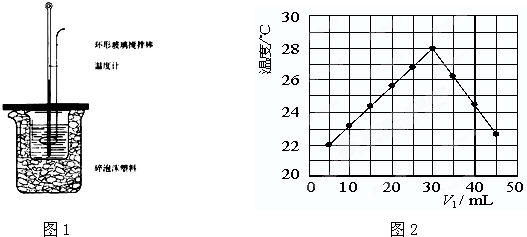
(1)大小烧杯间填满碎泡沫塑料的作用______.
(2)______(填“能”或“不能”)将环形玻璃搅拌棒改为环形铜棒.其原因是______.
(3)大烧杯上如不盖硬纸板,对求得中和热数值的影响是______(填“偏高”或“偏低”或“无影响”).
(4)如果改用60mL?1.0mol?L-1盐酸跟50mL?1.1mol?L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量______(“增加”、“减少”或“不变”),所求中和热数值______(“增加”、“减少”或“不变”)
(5)某研究小组将装置完善后,把V1?mL?1.0mol/L?HCl溶液和V2?mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图2所示(实验中始终保持V1+V2=50mL).回答下列问题:研究小组做该实验时环境温度______(填“高于”、“低于”或“等于”)22℃.
|