微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 可逆反应:I2(g)+H2(g) 2HI(g),在一定条件下已经达到平衡状态,由于改变浓度、温度、压强等条件中的一个,达到新平衡时,可能引起下列变化,这些变化中能说明平衡一定向正反应方向移动的是(???)
2HI(g),在一定条件下已经达到平衡状态,由于改变浓度、温度、压强等条件中的一个,达到新平衡时,可能引起下列变化,这些变化中能说明平衡一定向正反应方向移动的是(???)
①I2(g)浓度减小?②混合气颜色变浅?③I2(g)转化率增大?④HI(g)质量分数增大?⑤I2(g)+H2(g)质量分数减小
A.①②③
B.②③④
C.③④⑤
D.①③⑤
参考答案:C
本题解析:I2浓度减小,可能是由于从中取出部分I2,此时平衡向逆反应方向移动,同时混合气体颜色变浅。
本题难度:简单
2、选择题 下列说法中,正确的是
A.KW随溶液温度、浓度的改变而改变
B.凡是氧化还原反应,都是放热反应
C.对已达到化学平衡的反应,改变压强,平衡一定改变
D.弱电解质的电离程度,与温度、浓度均有关系
参考答案:D
本题解析:A:KW只与温度有关
B:例如高温下碳与二氧化碳的反应既属于吸热反应,也是氧化还原反应
C:当两边气体系数相等时,压强并不影响平衡
D:升温可促进电离,增加浓度,弱电解的电离度减小
答案为D
本题难度:一般
3、填空题 Ⅰ.(4分)在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g)?△H<0
CO2(g)+H2(g)?△H<0
(1)CO和H2O浓度变化如图,则0~4 min的平均反应速率ν(CO)=_______ mol/(L・min),此时该反应的平衡常数为???????????????????。
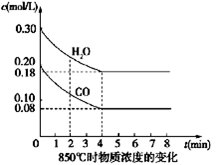
(2)当下列哪些物理量不再发生变化时,表明上述反应已达到平衡状态的是?????。
A.混合气体的压强
B.混合气体的密度
C.CO的物质的量浓度
D.密闭容器中放出热量
E.ν(CO)与ν(CO2)的比值
Ⅱ.(6分)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。
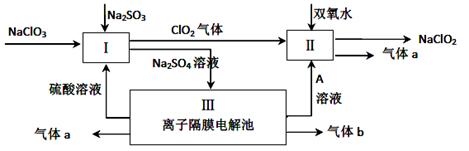
(3)配平Ⅰ中反应方程式 ?????ClO3-+????H++?????SO32-==?????ClO2↑+???SO42-+???????????
(4)A的化学式是??????,。生成气体a的电极反应式??????????????????????。
参考答案:Ⅰ.(4分)(1)0.03;(1分)1(1分)(2)CD (
本题解析:
试题分析:Ⅰ.(1)υ=?c÷?t=(0.20mol/l?0.08mol?L?1)÷4min =0.03mol/(L?min),
用三段式法计算:
CO(g)十H2O(g)?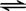 ?CO2(g)十H2?(g)
?CO2(g)十H2?(g)
起始:0.20mol/L? 0.30mol/L????0???????? 0
本题难度:困难
4、填空题 向某密闭容器中加入0.15mol/L A、0.05mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c( B)未画出,t1时增大到0.05mol/L]。乙图为 t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
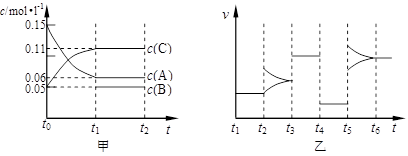
(1)若t4时改变的条件为减小压强,则B的起始物质的量浓度为??????????mol/L;
该反应的平衡常数表达式为K=?????????????????????。
(2)若t5时改变的条件是升温,此时v(正) > v(逆),平衡常数K的值将????????(选填“增大”、“减小”或“不变”)。
(3)若 t1= 15s,则t0~ t1阶段以C 浓度变化表示的平均反应速率为v(C)=??????????????
mol/L・s。t3时改变的某一反应条件可能是???????(选填序号)。
a.使用催化剂????? b.增大压强???c.增大反应物浓度????? d.降低产物浓度
(4)若A的物质的量减少0.02mol时,容器与外界的热交换总量为a kJ,写出该反应的热化学方程式????????????????????????????????????????????????????????????。
参考答案:(1)0.02 mol/L; (1分)?? K=[ B] ・
本题解析:
试题分析:
(1)根据甲图物质的变化量之比,可知A、C的计量数之比为3:2 ,t4时改变的条件为减小压强,但平衡不移动,说明左右两边气体分子数相同,因此B为生成物,系数为1,则起始浓度0.02 mol/L;?平衡常数表达式为K=[ B] ・[ C]2/ [ A]3。
(2)升温平衡正移,说明反应正向吸热,平衡常数K的值增大。?????
(3)v(C)= △c(C)/ △t=0.004mol/L・s??; t3时改变的某一反应条件,正逆反应速率增大,平衡不移动,只有a、 b 符合
本题难度:困难
5、选择题 在一固定容积的密闭容器中进行如下反应:2SO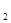 (g)+O
(g)+O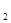 (g)
(g)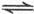 2SO
2SO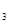 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO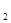 、O
、O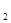 、SO
、SO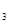 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
A.10秒时,用O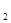 表示该反应的平均反应速率为0.01 mol/(L・s)
表示该反应的平均反应速率为0.01 mol/(L・s)
B.当反应达平衡时,SO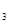 的物质的量可能为0.4 mol
的物质的量可能为0.4 mol
C.当SO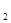 和O
和O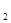 的生成速率之比为2:1时,达到该反应限度
的生成速率之比为2:1时,达到该反应限度
D.向容器内充人SO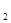 ,可以提高反应速率
,可以提高反应速率
参考答案:D
本题解析:
试题分析:反应进行到10s时生成三氧化硫0.2mol,则消耗氧气是0.1mol。由于不能确定容器的体积,所以不能计算该反应的反应速率是,A不正确;根据S原子守恒可知,SO2和SO3的物质的量之和是0.4mol,由于反应是可逆反应,反应物的转化率达不到100%,所以当反应达平衡时,SO3的物质的量不可能为0.4 mol,B不正确;反应速率之比是相应的化学计量数之比,所以二氧化硫和氧气的反应速率总是2:1的,C不正确;向容器内充人SO2,增大SO2的浓度,可以提高反应速率,D正确,答案选D。
点
本题难度:一般