微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是( )
A.电池内部含有电解质
B.锌是负极,碳棒是正极
C.电池用完后可埋入土壤
D.锌锰干电池属一次电池
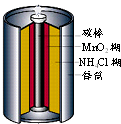
参考答案:A.锌锰干电池中氯化铵是电解质,故A正确;
B.锌锰干
本题解析:
本题难度:一般
2、简答题 将0.3mol?NaCl固体与0.1mol?CuSO4?5H2O固体混合溶于水,配成1000mL混合液.然后取出200ml溶液,用石墨作电极,通电一段时间.电解过程分为三个阶段试回答:
(1)其中第一阶段发生的电解反应的离子方程式为______.
(2)电解的最后一个阶段,阴极上发生的电极反应式变为______.
(3)若Cl-正好全部变为氯气逸出时,阴极上产生气体的体积______L(标准状况下)
参考答案:根据题意知,取出的溶液中含有的溶质的物质的量分别为:NaCl
本题解析:
本题难度:一般
3、选择题 下列有关原电池的说法正确的是
A.是把电能转化为化学能的装置
B.负极发生还原反应
C.正极失去电子
D.电流由正极经导线流向负极
参考答案:D
本题解析:
试题分析:A.原电池是把化学能转化为电能的装置,错误,B.原电池中电子流出的一极是负极,发生氧化反应,错误;C.原电池有两个电极,正极得电子,错误;D.电流由正极经导线流向负极,D正确;选D。
考点:考查原电池的工作原理。
本题难度:一般
4、选择题 控制适宜条件,将反应Sn(s)+Pb2+ (aq) Sn2+ (aq)+Pb(s)?△H<0,设计成如下图所示的原电池,一段时间后,灵敏电流计读数为零。则下列判断不正确的是( )
Sn2+ (aq)+Pb(s)?△H<0,设计成如下图所示的原电池,一段时间后,灵敏电流计读数为零。则下列判断不正确的是( )
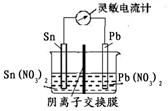
A.此时化学反应达到平衡状态
B.若此时将Sn电极换成质量较大的Sn 电极后,电流计指针偏转,c(Pb2+)将减小
C.若此时向左池加入少量的Sn(NO3)2固体,电流计指针偏转,Sn电极为正极
D.若此时升高温度,c(Sn2+)将减小,Pb电极为负极
参考答案:B
本题解析:
试题分析:灵敏电流计读数为零说明正逆反应进行的程度相同,反应达到平衡状态,故A正确;反应是放热反应,升高温度,平衡逆向进行,失电子的为负极,c(Sn2+)将减小,Pb电极为负极,故D正确;固体不影响平衡移动,若此时将Sn电极换成质量较大的Sn电极后,电流计指针不偏转,c(Pb2+)不变,故B错误;若此时向左池加入少量的Sn(NO3)2固体,溶解Sn2+浓度增大,平衡向逆反应移动,电流计指针偏转,Sn电极为正极,故C正确;故选B。
本题难度:一般
5、填空题 在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片口只发生电化学腐蚀,当在铜片上共放出2.24 L气体(标准状况)时,稀H2SO4刚好用去一半,则产生这些气体消耗锌___________g,共有___________mol电子通过导线,原H2SO4溶液的浓度是________mol/L
参考答案:6.5,0.20,1.0
本题解析:有关的电极反应为:负极Zn-2e-====Zn2+正极2H++2e-====H2↑n(H2)=0.10mol,则转移的电子为0.20mol,则n(Zn)=0.10mol,m(Zn)=6.5g。
c(H2SO4)=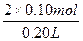 =1mol/L。
=1mol/L。
本题难度:简单