微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (13分)下图是元素周期表的一部分,其中所列字母分别代表某一元素
a
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| b
|
j
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| c
| d
| ?
| ?
|
?
| e
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| f
| ?
| ?
| g
| h
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| i
| ?
| ?
| ?
| ?
| ?
| k
| ?
| ?
| ?
| ?
|
(1)写出元素k基态原子的核外电子排布式________________________。
(2)e、f单质及ef形成的合金的硬度由大到小的顺序为_______________________(用具体名称回答)
(3)用来组成酸、碱、盐三类物质至少需要的元素有___________________(用表中列出元素的化学式填写)
(4)短周期某主族元素M的电离能情况如图(A)所示。则M元素位于周期表的第??????族。
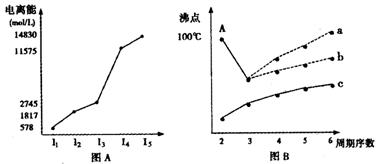
图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第????????族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线:折线a和折线b,你认为正确的是??????????。
2、填空题 (8分)现有部分短周期元素的性质或原子结构如下表:
元素编号
| 元素性质或原子结构
|
T
| 能形成双原子气体分子,原子中有三个单电子
|
X
| 核外有5个能级,最高能级上只有1个电子
|
Y
| 最外层电子数是次外层电子数2倍
|
Z
| 最高正价为+7价
(1)写出元素Z的离子结构示意图__________。另有某元素M在地壳中的含量仅次于X,写出其+2价阳离子的电子排布式?????。
(2)X的硫酸盐与过量氢氧化钡反应的离子反应方程式为__________。
(3)COZ2俗称光气,其中碳氧原子之间的共价键有????个σ键,???????个π键
(4)TH3的空间构型为 。???(填“难”或“易”)溶于CCl4。
3、填空题 A、B、C、D、E为五种原子序数依次增大的短周期主族元素。已知B的最外层电子数
与核外电子总数之比为3∶4;D的最外层电子数与次外层电子数之比为3∶4;E-、C+、A+的半径逐渐减小;常温下化合物AE为气体。
请回答下列问题:
(1)D、E的最高价氧化物对应水化物酸性较强的是________(写化学式)。
(2)用惰性电极电解化合物CE的饱和溶液,当电路中有0.2 mol电子通过时两极产生的气体在标准状况下的体积共________L。
(3)A与B、A与D均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式:________。
(4)化合物乙、丙均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1∶1∶1,乙溶液中水的电离程度比纯水的小。则化合物乙中的化学键类型为________;若丙为常见家用消毒剂的主要成分,则丙的化学式是________。
(5)均由A、B、C、D四种元素组成的两种盐发生反应的离子方程式是________;其中一种是强酸对应的酸式盐,写出向Ba(OH)2溶液中逐滴加入该盐溶液至中性发生反应的离子方程式:________。
4、选择题 下列叙述中,能说明金属M的金属性比金属N的金属性强的是
A.M原子的最外层电子数比N原子的最外层电子数少
B.常温时,M单质能从水中置换出氢气,而N单质不能反应
C.1mol M从稀H2SO4中置换出的H2比l mol N从稀H2SO4中置换出的H2多
D.在最高价氧化物的水化物中,M的化合价比N高。
5、填空题 现有3种化合物A、B、C均含短周期元素R,其转化关系如下图所示。
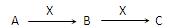
(1)若A由第三周期2种元素组成。常温下,0.1 mol/L X溶液的pH=13,则R在周
期表中的位置是???????????,X中阴离子的电子式是???????????,B转化为C的离子方程式是???????????。
(2)若常温下A、B、C、X均为气态物质,1 mol A中含有共价键的数目约为1.806×1024, X为单质,A与X反应生成B的化学方程式是???????????;在一定条件下,
A可与C反应消除C对大气的污染,该反应的化学方程式是???????????。
|