��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��д��ȷ���� [???? ]
A����Fe2(SO4)3��Һ�м��������Na2S:2Fe3+ +S2- ==2Fe2++S��
B����NH4Al(SO4)2��Һ�м���������Ba(OH)2��Һ��Al3++3OH-+Ba2++SO42-==BaSO4��+Al(OH)3��
C����ͭ���缫��ⱥ��ʳ��ˮ��2Cl-+2H2O Cl2��+H2��+2OH-
Cl2��+H2��+2OH-
D�����۵⻯����Һ�ڿ����б�����4I-+O2+H2O==2I2+4OH-
�ο��𰸣�D
���������
�����Ѷȣ���
2������� �ճ�����ˮ��NO3һ�ĺ�����ˮ�������������Ҫ��֮һ���ﵽһ��Ũ��ʱ������ཡ������Σ����Ϊ�˽�������ˮ��NO3һ��Ũ�ȣ�ij��ȤС��������·�����
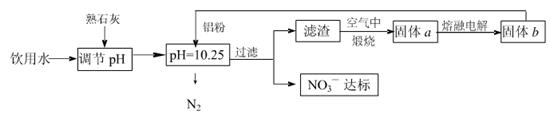
��ش��������⣺
��1���÷����ڵ���pHʱ����pH������С�������??????????�������ʽ��͡�
��2����֪���˺�õ�����Һ�м���������Ԫ�ء�������Һ�����ۺ�NO3һ��Ӧ�����ӷ���ʽΪ???????????????????????????????????????????????????????????��
�������ڿ��������չ������漰����ط�Ӧ����ʽΪ???????????????????????????????
��3����H2����ԭ��Ҳ�ɽ�������ˮ��NO3����Ũ�ȣ���֪��Ӧ�еĻ�ԭ���������������ɲ������ѭ���������ԭ�������ӷ���ʽΪ??????????????????????????��
��4������ˮ�е�NO3��??��Ҫ������NH4������֪�����������£�NH4��??����������Ӧ��������NO3��??��������Ӧ�������仯ʾ��ͼ���£�
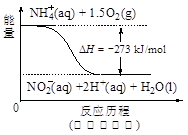 ???
???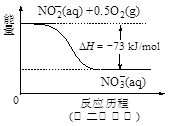
��д��1 mol NH4��?(aq)ȫ��������NO3��??(aq)���Ȼ�ѧ����ʽ��???????????????????��
��5������a���ڵ��ʱ������ӦʽΪ???????????????????????????????
�ο��𰸣���1��������Al��(2��)
��2����10Al+6NO3
���������
�����������1���������ܺ�����ܷ�Ӧ���÷����ڵ���pHʱ����pH������С�������������Al�� �������ʽ��͡���2������������������ӷ���������ԭ��Ӧ���ɹ��壬�����Ϊ���������������ᱻ��ԭΪ������������Һ�����ۺ�NO3����Ӧ�����ӷ���ʽΪ10Al+6NO3��+18H2O=10Al��OH��3+3N2��+6OH�����������ڿ��������չ������漰����ط�Ӧ����ʽΪ4Al+ 3O2 �����Ѷȣ�һ��
�����Ѷȣ�һ��
3��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�??��
A��AlCl3��Һ�м��������Ũ��ˮ:Al3++4NH3��H2O Al
Al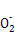 +4N
+4N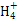 +2H2O
+2H2O
B����FeCl3��Һ��ʴͭ�ߵ�·��:Cu+2Fe3+ Cu2++2Fe2+
Cu2++2Fe2+
C������ʯ���ڴ����еķ�Ӧ:CaCO3+2H+ Ca2++H2O+CO2��
Ca2++H2O+CO2��
D������ˮ��Ӧ:Na+2H2O Na++2OH-+H2��
Na++2OH-+H2��
�ο��𰸣�B
���������AlCl3��NH3��H2O��Ӧ��������Al��OH��3������ƫ������,A��;C���е�CH3COOH���������,���ܲ��,��;D���ɣ����ӣ����غ�,ӦΪ2Na+2H2O 2Na++2OH-+H2����
2Na++2OH-+H2����
�����Ѷȣ�һ��
4��ѡ���� ������ط�Ӧ�����ӷ���ʽ��д��ȷ���ǣ�???��
A������������������Fe(OH)3 +3H+ ��Fe3++3H2O
B��NaHCO3��Һ�м��������Ba(OH)2��Һ��2HCO3��+Ba2++2OH�� = BaCO3? +2H2O+CO32��
C��NH4Al(SO4)2��Һ�м���Ba(OH)2��ҺʹSO42����ȫ������Al3+��2SO42����2Ba2+��4OH����AlO2����2BaSO4����2H2O
D������0.4 mol FeBr2����Һ��ͨ��0.1 mol Cl2��Ӧ��2Fe2++Cl2��2Fe3+ +2Cl��
�ο��𰸣�D
���������
���������A��Fe3����I�����ܹ��棬����B����ӦΪHCO3��+Ba2++OH�� = BaCO3? +H2O������C����ӦΪAl3����NH4����2SO42����2Ba2����4OH��=Al(OH)3����2BaSO4����NH3��H2O������ D��Fe2���Ļ�ԭ�Դ���Br������ȷ��
�����Ѷȣ�һ��
5��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽΪ
A��Ư����Һ�ڿ�����ʧЧ��ClO-��CO2��H2O=HClO��HCO3-
B��Fe3+��Һ�еμӹ����İ�ˮ�� Fe3++3OH����Fe(OH)3��
C��Cu2+��Һ�еμӹ����İ�ˮ�� Cu2++2NH3��H2O=Cu(OH)2��+2NH4+
D����1mol/L NaAlO2��Һ��1.5mol/L��HCl��Һ��������Ȼ�ϣ�
6AlO2��+9H��+3H2O��5Al(OH)3��+Al3��??
�ο��𰸣�D
���������Ư����Һ�ڿ�����ʧЧ����������̼��ƺʹ����ᣬ������ȶ����ֽ������������Ȼ��⣬A����ȷ����ˮ�����������ӷ���ʽ�в��ܸ�д�����ӵ���ʽ��B����ȷ������ˮ����ʱ��������ͭ���ܽ��ڰ�ˮ���γ������CuNH34(OH)2��C����ȷ������D��
�����Ѷȣ�һ��