微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于0.05mol/L的K2SO4溶液的说法中,正确的是
A.1L溶液中含有K+、SO42-总数为0.03NA
B.1L溶液中含有K+数目是0.1NA
C.1?L溶液中K+的浓度是0.20?mol/L
D.2?L溶液中含有SO42-的浓度是0.3mol/L
参考答案:B
本题解析:分析:A、根据n=cV计算硫酸钾的物质的量,每摩尔硫酸钾含有3mol离子(2mol钾离子,1mol硫酸根离子),再根据N=nNA计算离子的数目;
B、根据n=cV计算硫酸钾的物质的量,每摩尔硫酸钾含有3mol离子(2mol钾离子,1mol硫酸根离子),再根据N=nNA计算离子的数目;
C、每摩尔硫酸钾含有2mol钾离子,钾离子的浓度为硫酸钾的2倍;
D、溶液是均一的,每摩尔硫酸钾含有1mol硫酸根,硫酸根离子的浓度等于硫酸钾的浓度.
解答:A、1L溶液中所含K+、SO42-总数为1L×0.05mol/L×3×NAmol-1=0.15NA,故A错误;
B、1L溶液中含有K+离子数为1L×0.05mol/L×2×NAmol-1=0.1NA,故B正确;
C、0.05mol/L K2SO4溶液,每摩尔硫酸钾含有2mol钾离子,钾离子的浓度为硫酸钾的2倍,所以K+离子浓度是0.1mol/L,故C错误;
D、溶液是均一的,每摩尔硫酸钾含有1mol硫酸根,硫酸根离子的浓度等于硫酸钾的浓度为0.05mol/L,故D错误.
故选B.
点评:本题考查溶液物质的量浓度,比较基础,注意溶液是均一的,浓度与体积无关.
本题难度:一般
2、选择题 a?mol?O2气体和a?mol?O3气体相比较,下列叙述一定正确的是
A.体积相等
B.分子数相等
C.原子数相等
D.质量相等
参考答案:B
本题解析:分析:根据n=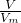 =
=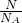 =
=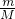 ,结合气体存在的外界条件是否一致和分子的组成解答.
,结合气体存在的外界条件是否一致和分子的组成解答.
解答:A、两种气体的物质的量相等,但气体存在的外界条件不一定相同,则体积不一定相等,故A错误;
B、由n=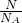 ,可知,气体的物质的量相等,则分子数相等,故B正确;
,可知,气体的物质的量相等,则分子数相等,故B正确;
C、两种气体的分子数相等,但分子中含原子数不等,则等物质的量时原子数不等,故C错误;
D、n=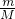 ,可知,两种气体的M不等,则等物质的量时气体的质量不等,故D错误.
,可知,两种气体的M不等,则等物质的量时气体的质量不等,故D错误.
故选B.
点评:本题考查物质的量的相关计算,题目难度不大,注意相关公式的运用,注意把握分子和原子的组成.
本题难度:一般
3、选择题 通过核磁共振氢谱可以推知(CH3)2CHCH2CH2OH有多少种氢原子[???? ]
A.6
B.5
C.4
D.3
参考答案:B
本题解析:
本题难度:一般
4、选择题 设NA为阿伏加德罗常数的值.下列说法正确的是
A.1?mol金刚石中含有的共价键数目为2NA
B.标准状况下,11.2?L甲醛中含有的氧原子数目为NA
C.1?L?0.1?mol?L-1?CH3COONa溶液中含有的阴离子总数为0.1NA
D.0.1?mol?Na2O2与足量水完全反应时,转移的电子数目为0.2NA
参考答案:A
本题解析:分析:A.金刚石中每个C原子形成四个共价键;
B.1mol甲醛中含有1mol氧原子;
C.水能发生微弱电离;
D.1?mol?Na2O2与水反应时转移1?mol电子.
解答:A.在金刚石中每个C原子形成四个共价键,但每个共价键为两个C原子共用,故A正确;
B.标准状况下11.2?L甲醛中含有氧原子数为0.5NA,故B错误;
C.水能发生微弱电离,阴离子总数大于0.1NA,故C错误;
D.1?mol?Na2O2与水反应时转移1?mol电子;0.1?mol?Na2O2与足量水完全反应时,转移的电子数目为0.2NA,故D错误.
故选A.
点评:本题考查阿伏加德罗常数,题目难度不大,注意从物质的组成、结构、性质、聚集状态以及存在的条件是否标准状况等角度思考.
本题难度:简单
5、选择题 下列化合物的核磁共振氢谱中出现三组峰的是 [???? ]
A. 2,2,3,3-四甲基丁烷
B. 2,3,4-三甲基戊烷
C. 3,4-二甲基己烷
D. 2,5-二甲基己烷
参考答案:D
本题解析:
本题难度:简单