微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有A、B、C、D四种强电解质,它们在水中电离产生的离子如下表(每种物质只含一种阴离子且互不重复).
A.B是NH4Cl
B.将等体积、等物质的量浓度的B溶液和C溶液混合,反应后的溶液c(Cl-)>c(Ba2+)
C.A的水溶液中可能有:c(OH)=c(HCO)+c(H+)+2c(H2CO3)
D.常温下,0.15?mol?L-1?C溶液和0.20?mol?L-1盐酸混合,所得混合液的pH=7,则C溶液和盐酸的体积比约为2:3
参考答案:B
本题解析:分析:根据①可知,A、B溶液中水的电离程度比纯水大,说明存在水解的离子,故A、B中含有的离子:一个含有NH4+、另一个含有CO32-,
根据②可知,B溶液和C溶液混合时只产生刺激性气味的气体,则该气体为NH3,为NH4+与OH-反应,故B、C中含有的离子:一个含有NH4+、另一个含有OH-.A、C溶液的pH均大于7,故C一定含有OH-,B含NH4+;C溶液和D溶液混合时只产生白色沉淀,只能为Ba2+与CO32-、SO42-,由于每种物质只含一种阴离子且互不重复,故C含有Ba2+,故C为Ba(OH)2,则D为Na2SO4、B为NH4Cl,故A含有CO32-,A溶液的pH均大于7,故Na2CO3或(NH4)2CO3,据此分析.
解答:根据①可知,A、B溶液中水的电离程度比纯水大,说明存在水解的离子,故A、B中含有的离子:一个含有NH4+、另一个含有CO32-,
根据②可知,B溶液和C溶液混合时只产生刺激性气味的气体,则该气体为NH3,为NH4+与OH-反应,故B、C中含有的离子:一个含有NH4+、另一个含有OH-.A、C溶液的pH均大于7,故C一定含有OH-,B含NH4+;C溶液和D溶液混合时只产生白色沉淀,只能为Ba2+与CO32-、SO42-,由于每种物质只含一种阴离子且互不重复,故C含有Ba2+,故C为Ba(OH)2,则D为Na2SO4、B为NH4Cl,故A含有CO32-,A溶液的pH均大于7,故Na2CO3或(NH4)2CO3,
A.由上述分析可知,B为NH4Cl,故A正确;
B.等体积、等物质的量浓度的B溶液和C溶液混合,钡离子、氯离子不发生反应,故所得溶液中c(Cl-)=c(Ba2+),故B错误;
C.若A为Na2CO3,溶液中氢氧根由水提供,水提供的氢离子,部分以氢离子形式存在、部分转化为碳酸氢根、碳酸分子,由水提供的氢氧根、氢离子相等可知,c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故C正确;
D.所得混合液的pH=7,则V[Ba(OH)2]×0.15?mol?L-1×2=V(盐酸)×0.2?mol?L-1,故V[Ba(OH)2]:V(盐酸)=2:3,故D正确;
故选B.
点评:本题考查离子及无机物推断,涉及离子反应、盐类水解、pH值有关计算等,题目难度中等,推断物质是解题的关键,没有信息中学一般不考虑弱酸弱碱盐的酸碱性判断.
本题难度:困难
2、选择题 元素周期表第二周期Li到Ne原子的电离能总的趋势是怎样变化的[???? ]
A.从大变小
B.从小变大
C.从Li到N逐渐增加,从N到Ne逐渐下降
D.没有多大变化
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列几种原子的基态电子排布,电负性最大的原子是( )
A.1s2?2s2?2p4
B.1s2?2s2?2p6?3s2?3p3
C.1s22s2?2p63s2?3p2
D.1s2?2s22p6?3s2?3p6?4s2
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列各组多电子原子的原子轨道能量比较不正确的是( )
A.3px=3pz
B.4s>3d
C.4p>3p
D.2s<2p
参考答案:B
本题解析:
本题难度:一般
5、填空题 元素周期表中前20号元素的第一电离能如图所示。试根据元素在周期表中的位置,分析表中曲线的变化特点,并回答下列问题。
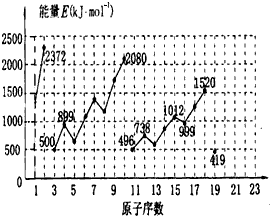
(1)同主族内不同元素的第一电离能变化的特点是______________________;各主族中第一电离能的这种变化特点体现了元素性质的______________________变化规律。
(2)同周期内,随原子序数增大,第一电离能增大。但个别元素的第一电离能出现反常现象,请分析其反常现象与原子结构的关系,预测下列关系式中正确的是___________(填写编号)
① E(砷)> E(硒) ② E(砷)< E(硒) ③ E(溴)> E(硒) ④ E(溴)< E(硒)
(3)估计Ca 原子的第一电离能[用E(Ca)表示]范围:_______< E(Ca)<________
(4)10号元素第一电离能较大的原因是_____________________________。
参考答案:(1)递减;周期性
(2)①③
(3)419;
本题解析:
本题难度:一般