微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2.某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物.已知SO3的熔点是16.8℃,沸点是44.8℃.
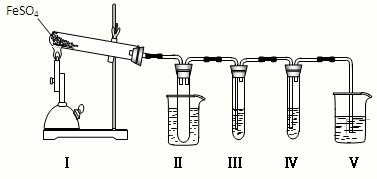
(1)装置Ⅱ的试管中不装任何试剂,其作用是______,试管浸泡在50℃的水浴中,目的是______.
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.限选试剂:3mol?L-1?H2SO4、6mol?L-1?NaOH、0.5mol?L-1?BaCl2、0.5mol?L-1?Ba(NO3)2、0.01mol?L-1酸性KMnO4溶液、0.01mol?L-1溴水.
| 检验试剂 | 预期现象和结论
装置Ⅲ的试管中加入______.
产生大量白色沉淀,证明气体产物中含有SO3.
装置Ⅳ的试管中加入______.
______
(3)装置Ⅴ的作用是防止尾气污染环境,烧杯中应加入的试剂是______.
参考答案:(1)Ⅰ中产生的气体极易和溶液反应时,会产生倒吸,所以装置I
本题解析:
本题难度:一般
2、实验题 某同学按如下实验流程提取海带中的碘,请回答相关问题。
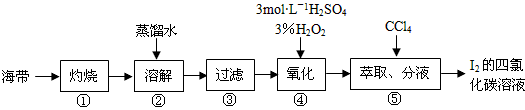
(1)第①步是将海带放入______________(填仪器名称)中,用酒精灯充分加热灰化。
(2)第②步为了加快溶解速度并使碘离子充分进入溶液,可以采取的措施是_____________________、
______________________(写出两条)。
(3)实验进行到某一步骤时应检验碘的存在,具体方法是_______________________________________________________________。
(4)海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第
_________步(填编号)与碘分离的。
参考答案:(1)坩埚
(2)充分搅拌;加热煮沸
(3)取氧
本题解析:
本题难度:一般
3、选择题 下列实验设计和结论相符的是 [???? ]
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.因为HCl难溶于饱和食盐水,故实验室可用排饱和食盐水法收集HCl
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列实验或操作合理的是[???? ]
A.制氨气 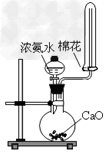 ?????? ??????
B.蒸发、结晶 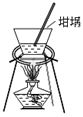 ????????? ?????????
C.萃取碘???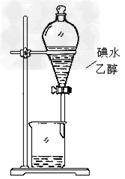
D.用酸性KMnO4溶液滴定 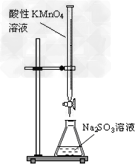
参考答案:AD
本题解析:
本题难度:一般
5、简答题 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算.实验中加热至恒重的目的是______.
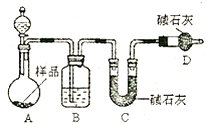
(2)方案二:按图装置进行实验.并回答以下问题.
①实验前先______.分液漏斗中应该装______(“盐酸”或“硫酸”).
D装置的作用是______.
②实验中除称量样品质量外,还需称______装置前后质量的变化.
③根据此实验得到的数据,测定结果有误差.因为实验装置还存在一个明显缺陷,该缺陷是______.
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液.过滤洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯,漏斗外,还用到的玻璃仪器有______.
②实验中判断沉淀是否完全的方法是______.
③已知称得样品21.2g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为______.
参考答案:(1)该方案根据加热后残渣的质量来求解,要加热至恒重,以保证
本题解析:
本题难度:一般
|