��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ����
A��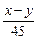
B��
C��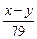
D��
�ο��𰸣�A
�����������������ijԪ�ص����ԭ��������һ��ֵ����ʽ��⡣x��62n=y��17n?n=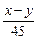 ��
��
�����Ѷȣ�һ��
2��ʵ���� ͼ������ʵ���ҽ��а��������Ʊ�������ʵ������װ�ã����̶ֹ�װ��δ������
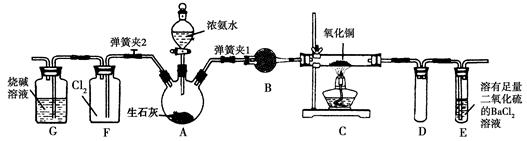
(1)����װ��װ�ú���Ҫ����A��Eװ�õ������ԣ������������________��Ȼ����A���۲쵽E��������ð�����ƿ��ƾ��ƻ��ɿ�˫�֣�E�е�����ˮ���γɣ�˵��װ�����������á�
(2)װ��B��ʢ�ŵ��Լ���________��
(3)��ȼC���ƾ��ƣ��رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©�����Ժ�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ����________(������)����E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ��________________________��
(4)��C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16 g����Ӧ����ع�����������2.4 g��ͨ������ȷ���ù������ijɷ���_________
__________(�û�ѧʽ��ʾ)��
(5)�ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�У�д���������̵Ļ�ѧ����ʽ��____________________��Ѹ�ٲ���������ԭ����____________________________��
�ο��𰸣�(1)�رյ��ɼ�2�ͷ�Һ©�����������ɼ�1����E��װ��ˮ
���������A���Ʊ�NH3��װ�ã�B�Ǹ���NH3��װ�ã�C��NH3��CuO�ķ�Ӧװ�ã�E�Ǵ���NH3��β��װ�ã�F��NH3��Cl2�ķ�Ӧװ�ã�G�Ǵ���β��Cl2��װ�á�
(2)����NH3��ʹ�ü��Ը������(3)C��CuO��NH3����������ԭ��Ӧ���ɺ�ɫ��Cu��N2��H2O��E�з�����Ӧ��2NH3��BaCl2��SO2��H2O=BaSO3����2NH4Cl��(4)������ȫ����Cu�����ɲ�����֪��С�IJ���ȫ����OԪ�ص���������n(CuO)��n(O)��2.4 g��16 g��mol��1��0.15 mol�����Է�Ӧ��CuO��
�����Ѷȣ�����
3��ѡ���� ���ʵ���֮��Ϊ2�U5��п��ϡ���ᷴӦ�������ᱻ��ԭ�IJ���ΪN2O����Ӧ������пû��ʣ�࣬��÷�Ӧ�б���ԭ��������δ����ԭ����������ʵ���֮����
A��1�U4
B��1�U5
C��2�U3
D��2�U5
�ο��𰸣�A
���������
�����������п�����ʵ���Ϊ2molʱ����������п�����ʵ���Ϊ2mol��δ����ԭ����������������Ӿ�����������п�У���δ����ԭ������Ϊ4mol����Ӧ����пΪ5mol������ԭ��Ϊ1mol���ʱ���ԭ��������δ����ԭ����������ʵ���֮��Ϊ1:4,����ѡA��
�����Ѷȣ�һ��
4��ʵ���� ij����С�����������ʵ�鷽����֤Ag��ŨHNO3��Ӧ�Ĺ����п��ܲ��� NO����ʵ������ͼ���£�
NO����ʵ������ͼ���£�

�Ųⶨ��������ʵ���
��Ӧ��������ͼBװ��������100 mL��Һ��ȡ��25.00 mL��Һ����0.1 mol��L��1��NaOH��Һ�ζ����÷�̪��ָʾ�����ζ�ǰ��ĵζ�����Һ���λ������ͼ��ʾ����B������������������ʵ���Ϊ____________����Ag��Ũ���ᷴӦ���������ɵ�NO2�����ʵ���Ϊ______________��
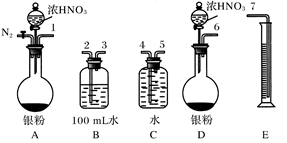
�ƲⶨNO�����
�ٴ���ͼ��ʾ��װ���У�����ΪӦѡ��________װ�ý���Ag��Ũ���ᷴӦʵ�飬ѡ�õ�������____________________________________________________________
________________________________________________________________________��
��ѡ����ͼ��ʾ�������һ�������ⶨ����NO�����װ�ã������������˳����_________________________(������ܿڱ��)��
���ڲⶨNO�����ʱ������Ͳ��ˮ��Һ��ȼ���ƿ��Һ��Ҫ�ͣ���ʱӦ����Ͳ��λ��______(ѡ��½��������ߡ�)���Ա�֤��Ͳ�е�Һ���뼯��ƿ�е�Һ���ƽ��
������ɷַ���
��ʵ����NO�����Ϊ112.0 mL(�����㵽��״��)����Ag��Ũ���ᷴӦ�Ĺ�����________(��С���û�С�)NO�����������жϵ�������__________________
________________________________________________________________________��
�ο��𰸣�(14��)��0.008 mol ??��2�֣�???? 0.0
�����������
�����Ѷȣ�һ��
5������� ��ҵ����ȡ����淋�����ͼ���£���ش��������⣺
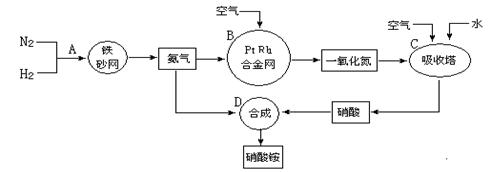
��1����������ҵ������������У�B�豸��������?????????????�����з�����Ӧ�Ļ�ѧ����ʽΪ????????????????????????????????????????????????????��
��2�������������У�N2��H2�ϳ�NH3���õĴ�����??????????????��1909�껯ѧ�ҹ�����ʵ�����״κϳ��˰���2007�껯ѧ�Ҹ���¡����ض��ڹ����о���֤ʵ�������뵪���ڹ����������ϳɰ��ķ�Ӧ���̣�ʾ��ͼ���£�

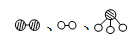 �ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ���????????????????��????????????????????��
�ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ���????????????????��????????????????????��
��3���ںϳɰ����豸���ϳ������У������Ƚ�������Ŀ����?????????????????????���ںϳ��������������ͨ�������Ŀ����??????????????????????????????��
��4����������Ĺ����г������һЩ��������������������ַ���������
��Һ���շ���NO��NO2��2NaOH��2NaNO2��H2O
NH3��ԭ����8NH3��6NO2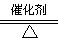 ?7N2��12H2O��NOҲ�����Ƶķ�Ӧ��
?7N2��12H2O��NOҲ�����Ƶķ�Ӧ��
�������ַ����У�������ɫ��ѧ����???????????????????????????????????��
��5��ij���ʳ���NH3�Ʊ�NH4NO3����֪����NH3��NO�IJ�����96%��NO��HNO3�IJ�����92%������HNO3����ȥ��NH3������ռ�ܺ�NH3������������������ģ�����??????%��
��6���������һ�ֳ��õĵ��ʣ��������ʹ�øû���ʱ��Ӧע�����������ǣ�
?
| ע������
| ����
|
��
| ?
| ?
|
��
| ?
| ?
?
�ο��𰸣���1������¯����1�֣�????? 4NH3+5O2![]()
���������
�����������1����ҵ�������ð���������ȡ���䷨���Ϳ���Ϊԭ�ϣ���Pt��Rh�Ͻ���Ϊ����������¯���� 800�����������Ӧ�����ɵ�NO����ȴʱ��O2��NO2��NO2������������ˮ�����ڹ���������O2��������ת��Ϊ���ᣬ���Ũ�ȿɴ�50������Ũ�������50��HNO3��Mg[NO3]2��ŨH2SO4������á���Ӧ�Ļ�ѧ����ʽ�ֱ�Ϊ��4NH3+5O2 �����Ѷȣ�һ�� �����Ѷȣ�һ��
|