微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用稀硫酸、氨水、氢氧化钠溶液中的任何一种作为试剂,均可鉴别的一组试剂是
A.NaCl和Na2CO3
B.BaCl2和FeCl2
C.FeCl2和FeSO4
D.Al2(SO4)3和AlCl3
参考答案:B
本题解析:A,氨水、氢氧化钠不能鉴别;B,稀硫酸与BaCl2溶液反应先产生白色沉淀,与FeCl2溶液不反应,可以鉴别;氨水与FeCl2溶液反应有颜色变化,与BaCl2溶液不反应,无明显现象,因而可以鉴别;氢氧化钠溶液与FeCl2溶液反应产生白色絮状沉淀,最后变为红褐色,与BaCl2溶液无明显现象,也可以鉴别;C,FeCl2、FeSO4都与稀硫酸不反应,无法鉴别;D,氨水与Al2(SO4)3、AlCl3反应都产生白色沉淀;氢氧化钠溶液与Al2(SO4)3、AlCl3反应都先产生白色沉淀,然后沉淀溶解;综上所述,答案为B。
本题难度:简单
2、实验题 为了测定酶的专一性,我们做如下实验:
①用清水 将口漱净,口内含一块消过毒的脱脂棉,用镊子取出脱脂棉,将其中的唾液收集到小烧杯中;
②稀释;
③取两支洁净的试管,编上号,做如下操作:向试管1注入可溶性淀粉溶液2 mL,加入稀释唾液2 mL, 向试管2注入蔗糖溶液2 mL,加入稀释唾液 2 mL;
④轻轻振荡并保持试管的下半部分浸入 37℃温水中10 min;
⑤加入2 mL Cu(OH)2悬浊液;
⑥将试管下半部分放在酒精灯上均匀加热,煮沸5~10 min;
⑦10 min后1号试管中有红色沉淀 (Cu2O)生成。
请回答:
(1)为什么要将试管的下半部分浸到37℃的温水中______________?
(2)对步骤⑦,说明现象出现的原因___________。
(3)比较试管1、2的最终现象,本实验能说明什么问题_____________?
参考答案:(1)使酶具有最高的催化效率。
(2)nH2O+ 2(
本题解析:
本题难度:一般
3、实验题 已知浓硫酸具有强氧化性,可与炭粉反应。
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式:___________________
(2)试用如图所示装置设计一个实验来验证上述反应所产生的各种产物。这些装置的连接顺序是
_____→_____→______→_______(填编号)。

(3)装置②中所加固体药品是____,可确定的产物是____。确定装置②在整套装置中的位置,理由是____________________。
(4)③中所盛溶液是____,可验证的产物是___。
参考答案:(1)C+2H2SO4(浓)![]() 本题解析:
本题解析:
本题难度:一般
4、实验题 (1)在硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行
???????次。
(2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、??????????、??????????。
(3)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。
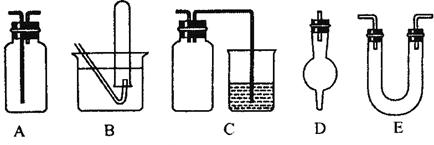
请回答下列问题:
①能用作干燥氨气的装置有_______________(填字母);
②既能用于收集氯气又能用于收集一氧化氮气体的装置有_______________(填字母);
③在实验室制备氯气的实验中,用以除去氯气中氯化氢等杂质气体的装置有________________ (填字母);
④能用于乙烯与溴水反应制二溴乙烷的实验装置有__________(填字母);
⑤在C装置中,若用烧杯内的氢氧化钠溶液吸收尾气二氧化硫,则广口瓶的作用是___________________。
(4)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了右图所示的实验。
①可通过观察??????????????来定性的得出结论;
②有A同学提出将CuSO4改为CuCl2更为合理,其理由是??????????;
若不采用A同学的改进方案,你认为还可以如何改进?????????????。
参考答案:(1)4??(1分)(2)环形玻璃搅拌棒(不答环形不得分)、
本题解析:
试题分析:(1)在CuSO4晶体结晶水测定的实验中至少4次称量,分别为:坩埚质量、坩埚和样品质量、灼烧后坩埚和样品质量、再灼烧后坩埚和样品质量。
(2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、环形玻璃搅拌棒、量筒。
(3)①氨气为碱性气体,常用碱性干燥剂碱石灰固体干燥,而碱石灰只能填装在D、E中,。
②一氧化氮易与氧气反应,只能用排水法收集。氯气的密度大于空气的,可以用向下排空气法或还饱和食盐水法收集,所以答案选B。
③除去氯气中氯化氢等杂质气体的装置应为洗气瓶,A长用作洗气瓶,故答案为A。
(4)①比较反应速率的大小可通过生成气体的快慢来判断,因此正确的答案是反应产生气泡快慢或反应完成的先后或试管壁的冷热程度。
②比较不同催化剂的催化效果,应排除其它因素的干扰。由于CuSO4、FeCl3中的阴离子不同,不能排除阴离子的因素,所以将FeCl3改为Fe2(SO4)3或将硫酸铜改为氯化铜均可以。
点评:该题是高考中的基本实验题,属于中等难度的试题。本题涉及化学实验操作、气体的净化、收集实验安全、实验探究的等问题,注意A瓶,可用作集气瓶、洗气瓶、安全瓶、量器瓶等,有利于培养学生的综合实验能力,有助于提升学生的学科素养,提高学生的学习效率。
本题难度:一般
5、实验题 某研究性学习小组设计实验方案制备氯化铜并验证次氯酸的漂白性。
已知氯化铜遇水蒸气潮解。
?
?
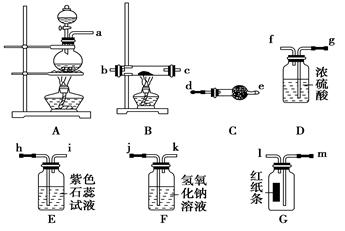 根据上述仪器组合装置,回答下列问题: 根据上述仪器组合装置,回答下列问题:
(1)组装实验装置:气体流向从左至右,导管口的连接顺序为__________________。
(2)为了防止空气与铜粉反应,先点燃________处酒精灯,当___________________时,再点燃另一酒精灯。
(3)D装置的作用是________________________,
F装置的作用是_________________ __________。 __________。
(4)能证明氯气没有漂白性,次氯酸有漂白性的实验现象________________________________________________________________________。
(5)本实验方案没有除去氯气中的氯化氢,对实验有无影响?________;理由是
_______________________________________________________________________ _。 _。
参考答案:(1)a→gf→bc(cb)→ml→hi→jk (3分)
本题解析:略
本题难度:一般
|