微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X、Y、Z和W代表原子序数依次增大的4种短周期元素.X元素原子最外层电子数比次外层电子数多1;Z与Y相邻,Z比Y的电子数多8;W元素原子最外层电子数等于电子层数的2倍.下列说法正确的是( )
A.原子半径Y>Z>W
B.Y、Z和W三种元素位于同一周期
C.Y元素最高价氧化物对应的水化物一定是强酸
D.Y、Z的最高正价与最低负价绝对值之和均为8
参考答案:D
本题解析:
本题难度:简单
2、填空题 (8分)A、B、D、E是短周期中构成蛋白质的重要元素,其性质见下表。Fe、Co元素的常见化合价为+2、+3,能形成各种有色配离子。
?
| A
| B
| D
| E
|
化合价
| -4
| -2
| -3
| -2
|
电负性
| 2.5
| 2.5
| 3.0
| 3.5
(1)基态Fe原子的电子排布式为??????????????。
(2)Fe、Co两元素的第三电离能I3(Fe)???I3(Co)(填“<”或“>”)。
(3)B、D、E的气态氢化物的沸点由高到低的顺序为?????????????????(填化学式)。
(4)Co与E形成的化合物晶胞如右图所示,则该化合物的化学式为????????。(用元素符号表示)
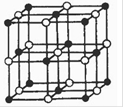
(5)Co的离子能与AD-离子生成各种配合物。紫色的配离子[Co(AD)6]4-是一种相当强的还原剂,在加热时能与水反应生成[Co(AD)6]3-。???
①HAD分子中A元素的杂化类型为?????,D元素的化合价为???。
②写出[Co(AD)6]4-在加热时与水反应生成[Co(AD)6]3-的离子方程式:??????????????。
参考答案:(1)1s22s22p63s23p63d64s2(1分)??
本题解析:(1)根据构造原理可知,基态Fe原子的电子排布式为1s22s22p63s23p63d64s2。
(2)由于亚铁离子失去电子生成铁离子后,3d轨道电子是半充满状态,稳定性强,所以Fe、Co两元素的第三电离能是I3(Fe)>I3(Co)。
(3)根据元素的性质可知,A、B、D、E分别是C、S、N、O。由于水分子和氨气分子间都存在氢键,沸点高,所以气态氢化物的沸点由高到低的顺序为H2O>NH3>H2S。
(4)根据晶胞的结构可知,含有的原子个数分别是12×1/4+1=4、8×1/8
本题难度:一般
3、选择题 下列叙述正确的是? [???? ]
A.蛋白质、人造纤维和光导纤维都属于有机高分子化合物
B.化学反应的过程可以看做是储存在物质内部的能量转化为热、电、光能等释放出来或者是热、电、光能等转化为物质内部的能量被储存起来的过程
C.共价键是原子间通过共用电子对形成的,离子键是阴、阳离子问通过静电吸引力形成的 D.合金材料都是由两种或两种以上金属元素组成的
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列叙述正确的是
[???? ]
A.非金属原子间以共价键结合的物质都是共价化合物
B.含有共价键的化合物都是共价化合物
C.凡是能电离出离子的化合物都是离子化合物
D.凡是含有离子键的化合物都是离子化合物
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列描述中正确的是?? ( )
A.CS2分子的立体构型为V形
B.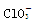 的空间构型为平面三角形 的空间构型为平面三角形
C.SF6中有每个原子均满足最外层8电子稳定结构
D.SiF4和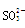 的中心原子均为sp3杂化 的中心原子均为sp3杂化
参考答案:D
本题解析:
试题分析:A中中心原子碳原子不存在孤对电子,所以是直线型结构,A不正确;微粒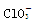 中中心原子的孤对电子对数是(7+1-3×2)÷2=1,所以是三角锥形结构,B不正确;C不正确,S原子不能满足8电子稳定结构,所以正确的答案选D。 中中心原子的孤对电子对数是(7+1-3×2)÷2=1,所以是三角锥形结构,B不正确;C不正确,S原子不能满足8电子稳定结构,所以正确的答案选D。
点评:该题是中等难度的试题,试题难易适中,贴近高考。侧重对学生解题能力和方法
本题难度:一般
|