微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知断裂1 mol H―H键吸收的能量为436 kJ,断裂1 mol H―N键吸收的能量为391 kJ,根据化学方程式:N2(g)+3H2(g)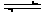 2NH3(g) ΔH=-92.4 kJ・mol-1,则断裂1 mol N≡N键吸收的能量是
2NH3(g) ΔH=-92.4 kJ・mol-1,则断裂1 mol N≡N键吸收的能量是
A.431 kJ
B.945.6 kJ
C.649 kJ
D.869 kJ
参考答案:B
本题解析:
试题解析:已知:H-H键能为436kJ/mol,H-N键能为391kJ/mol,设N≡N的键能为x,对于反应N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,反应热=反应物的总键能-生成物的总键能,
故x+3×436kJ/mol-2×3×391kJ/mol=-92.4kJ/mol,解得:x="945.6" kJ/mol故选B.
考点:有关反应热的计算
本题难度:一般
2、选择题 某致基因突变物质的结构简式如图。下列相关分析正确的是
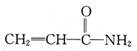
A.电负性:C<N<O
B.该分子中σ键与π键数目之比为4:2
C.该分子所有原子处于同一平面
D.该分子的加聚产物为
参考答案:A
本题解析:
试题分析:A、同周期主族元素,随着原子序数的增大,电负性增大,所以电负性:C<N<O,正确;B、根据结构简式可知,该分子中σ键9个,π键2个,二者数目之比为9:2,错误;C、N原子与周围的原子不在同一平面上,错误;D、加聚后主链为―CH2―CH―,错误。
本题难度:一般
3、选择题 关于氢键,下列说法正确的是(?????)
A.氢键比分子间作用力强,所以它属于化学键
B.冰中存在氢键,水中不存在氢键
C.分子间形成的氢键使物质的熔点和沸点升高
D.H2O是一种非常稳定的化合物,这是由于氢键所致
参考答案:C
本题解析:氢键远低于化学键键能,属于分子间作用力,但它可以提高分子熔点和沸点;水分子中的H―O键保证了水是一种稳定的化合物;水和冰中均存有氢键。
本题难度:一般
4、选择题 下列物质中,既含有离子键又含有共价键的是
A.CH4
B.NaOH
C.SO2
D.H2O
参考答案:B
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。据此判断A~D中含有的化学键分别是极性键、离子键和极性键、极性键、极性键,所以答案选B。
本题难度:一般
5、选择题 近年来研制的NF3气体可用作氟化氢―氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2=NF3+3NH4F,下列说法中不正确的是( )
A.NF3的形成过程用电子式可表示为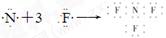
B.NF3分子空间构型为三角锥形
C.NF3的氧化性大于F2
D.NH4F中既有离子键又有极性共价键
参考答案:C
本题解析:
试题分析:氮元素和氟元素均是活泼的非金属,二者形成的化学键是极性键,即NF3是含有共价键的共价化合物,A正确;NF3分子空间构型与氨气的类似,均是三角锥形结构,B正确;NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2=NF3+3NH4F,乙醇氟气的氧化性强于NF3的,选项C不正确;NH4F与氯化铵的结构是相似的,既有离子键又有极性共价键,选项D正确,答案选C。
点评:该题以NF3为载体,重点考查学生的化学键、化合物的形成过程以及氧化还原反应的有关应用,有利于调动学生的学习兴趣,激发
本题难度:简单