��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ѧ��Ӧ���ʵ���Ҫ�����ǣ�??��
A����Ӧ���Ũ��
B����Ӧ��ϵ�ڵ�ѹǿ
C����Ӧ�������
D����Ӧ���״̬
�ο��𰸣�C
���������
���������������ѧ��Ӧ���ʵ���Ҫ�����ǣ���Ӧ�ﱾ�������ʡ�ѡC��
�����Ѷȣ���
2��ʵ���� ��14�֣�ij������ȤС���˫��ˮ��H2O2ˮ��Һ����������ʵ��̽����
��1����������ͬ���ۼ�״̬��ͬ��MnO2�ֱ����5mL 5%��˫��ˮ�У����ô����ǵ�ľ����֮���ⶨ������£�
������MnO2��
| �������
| �۲���
| ��Ӧ��������ʱ��
|
��ĩ״
| ��ϲ���
| ���ҷ�Ӧ��ʹľ����ȼ
| 3.5����
|
��״
|
| ��Ӧ����,���Ǻ�����ľ��δ��ȼ
| 30����
��д��H2O2��Ӧ�Ļ�ѧ����ʽ ��
��ʵ����˵���������õĴ�С�� �йء�
��2��ȡ���ݺ��е���H2O2��������������ͬ��˫��ˮ���ֱ������м���1��MnO2��ĩ���ⶨ������£�
˫��ˮ���
| �������
| ��Ӧ��������ʱ��
| �ռ����������
| ��Ӧ��Һ���¶�
| a1%��150mL
|
| 11����
| 539mL
| 24��
| a2%��15mL
| ��ϲ���
| 1��20��
| 553mL
| 56��
| a3%��7.5mL
|
| 9��
| 562mL
| 67��
���Ҫ˵����
�ٷ�Ӧ��������ʱ�䲻ͬ��ԭ�� ��
�ڷ�Ӧ��Һ���¶Ȳ�ͬ��ԭ�� ��
���ռ������������ͬ��ԭ�� ��
��3�����з�̪��NaOHϡ��Һ�У���ε���10% ��˫��ˮ����ɫ��ȥ��
����֪˫��ˮ�������ԣ���д��H2O2�ĵ��뷽��ʽ�� ��
��С�����ۺ�ɫ��ȥ��ԭ��ʱ����ͬѧ��Ϊ��˫��ˮ���������£���ͬѧ��Ϊ��˫��ˮ�н�ǿ���������¡��������һ����ʵ����˵���ǼԻ����Ҷԡ�����Ҫ����˵��)
�ο��𰸣���ÿ��2�֣���14�֣�
��1���� �����������1����˫��ˮ�ڴ����������£��ֽ�������������Ӧ�ķ���ʽ��2H2O2 �����������1����˫��ˮ�ڴ����������£��ֽ�������������Ӧ�ķ���ʽ��2H2O2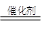 2H2O��O2���� 2H2O��O2����
�ڸ��ݷ�Ӧ��������ʱ����жϣ��������õĴ�С������ı�������ۼ�״̬���й�ϵ��
��2����������Һ������������ͬ��ͬʱ��Һ���¶Ȳ�ͬ���Ӷ����·�Ӧ���ʲ�ͬ�����Է�Ӧ��������ʱ�䲻ͬ��
������˫��ˮ��������ͬ�����Է�Ӧ�ų�������ͬ����Һ�������ͬ��������Һ���¶��Dz�ͬ�ġ�
������Һ�������ͬ����Һ���¶Ȳ�ͬ���Ӷ�Ӱ����������Һ�е��ܽ����������ռ����������Dz�ͬ�ġ�
��3����˫��ˮ���Կ����Ƕ�Ԫ���ᣬ�����Ƿֲ��ģ���H2O2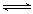 HO2����H����H2O2 HO2����H����H2O2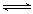 HOO����H������ HOO����H������
�������˫��ˮ�н�ǿ���������£����ټ�������������Һ���Dz����Ժ�ɫ�ģ��Ӵֿ��Լ��𣬼�����ɫ��Һ������μ���NaOH��Һ������ɫ�ָ�˵���ԣ�����ɫ���ֵ���˵���Ҷԡ�
�����Ѷȣ�����
3��ѡ���� ���������ķ�Ӧ�У���ʹ��Ӧ���л�������ͻ���Ӱٷ���ͬʱ����ķ�����
������Ӧ���Ũ�� �������¶� ������ѹǿ ����ȥ������ �ݼ������
A���٢ڢ�
B���٢ڢۢ�
C���ڢ�
D���٢ڢۢܢ�
�ο��𰸣�C
���������
�������������Ӧ���Ũ�Ⱥ�����ѹǿ��ֻ�������������������������Ӱٷ������������¶Ⱥͼ���������������������������������Ӱٷ�������ȥ�����Ũ�Ƚ��ͣ��������Ŀ��С��
���㣺��������Է�Ӧ���ʵ�Ӱ��
�����Ѷȣ�һ��
4��ѡ���� �ڷ�ӦCuO+H2SO4�TCuS04+H2O�У��ɼӿ췴Ӧ���ʵĴ�ʩ�ǣ�������
A����ˮ
B�������¶�
C��.����ѹǿ
D�������¶�
�ο��𰸣�A����ˮ��������Ũ�ȼ�С����Ӧ���ʼ�С����A����
B
���������
�����Ѷȣ���
5��ѡ���� ��þ��Ͷ��ʢ������ij��������У������������ʱ仯��ͼ��ʾ�����������У�Ӱ�췴Ӧ���ʵ�������
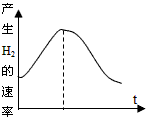
[???? ]
�������Ũ�� ��þ���ı���� ����Һ���¶� ��Cl-��Ũ��
A���٢�
B���ۢ�
C���٢ڢ�
D���ڢ�
�ο��𰸣�C
���������
�����Ѷȣ�һ��
|
|