微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将质量分数为0.052(5.2%)的NaOH溶液1升(密度为1.06克/毫升)用铂电极电解,当溶液中的NaOH的质量分数改变了0.010(1.0%)时停止电解,则此时溶液中应符合的关系是
| NaOH的质量分数 | 阳极析出物的质量(克) | 阴极析出物的质量(克)
①
0.062(6.2%)
19
152
②
0.062(6.2%)
152
19
③
0.042(4.2%)
1.2
9.4
④
0.042(4.2%)
9.4
1.2
( )
A.①
B.②
C.③
D.④
2、填空题 (14分)
如下图所示,A、F为石墨电极,B、E为铁片电极.按要求回答下列问题.
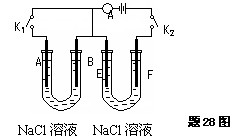
(1)打开K2,合并K1.B为?????极,A的电极反应为????????????????,最终可观察到的现象是???????????????????????????????????????????????????.
(2)打开K1,合并K2.E为???????极,F极的电极反应为???????????????????????,
检验F极产生气体的方法是???????????????????????????????????????.
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是???????????????????????,原因是????????????????????????????????.
3、填空题 能源是人类生活和社会发展的物质基础,研究化学反应中的能量变化,有助于更好地利用化学反应为人们的生产和生活服务。回答下列问题:
(1)从能量的角度看,断开化学键要____,形成化学键要___。已知拆开1 mol H-H键、1 mol I-I键、1 mol H-I键分别需要吸收的能量为436 kJ、151 kJ和299 kJ。则由氢气和碘反应生成1 mol HI需要___kJ 的热量(注明“放出”或“吸收”)。
(2)在生产和生活中经常遇到化学能与电能的相互转化。在如图甲所示的装置中,负极的电极反应式为______,总反应方程式为___。 Cu片附近pH____。当导线中有2 mol e-通过时,理论上两极的变化是:负极溶解了___g锌,正极上生成___g氢气。
(3)乙装置中铝电极作____极,被____(填“氧化”或“还原”)。?

4、选择题 下列关于铜电极的叙述,正确的是 [???? ]
A.铜锌原电池中,铜是正极
B.用电解法精炼粗铜时,粗铜作阴极
C.在镀件上电镀铜时,可用金属铜作阴极
D.电解稀硫酸制H2、O2时,铜作阳极
5、选择题 下列叙述正确的是
A.电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过
B.在铁上镀锌时,锌棒作阳极,且电解液硫酸锌的浓度是不变的
C.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1: 2
D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
|