微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中正确的是( )
A.等物质的量浓度NaCl和CH3COONa溶液等体积混合,
c(Cl-)>c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.25℃时,若10mL盐酸(pHa)与100mLBa(OH)2溶液(pHb)混合后恰好中和,则pHa+pHb=13
C.等物质的量浓度的硫酸与醋酸钠溶液等体积混合,c(SO42-)+c(OH-)=c(H+)+c(CH3COOH)
D.向氨水中加水稀释,
c(NH
+4
)
c(NH3?H2O)
减小
参考答案:A、等物质的量浓度NaCl和CH3COONa溶液中,醋酸根离
本题解析:
本题难度:简单
2、选择题 在醋酸溶液中,CH3COOH电离达到平衡的标志是
A.溶液显电中性
B.溶液中检测不出CH3COOH分子存在
C.氢离子浓度恒定不变
D.c(H+)=c(CH3COO-)
参考答案:C
本题解析:电离平衡为:CH3COOH CH3COO―+H+ CH3COO―+H+
溶液本身就是电中性,排除A;由于醋酸为弱电解质,不可能全部电离,所以溶液中任何时间都能检测出CH3COOH分子,排除B;在电离过程中c(H+)与c(CH3COO-)任何时候都相等,也不能做为平衡标志,排除D;故答案为C:当氢离子浓度不变时,电离达到平衡
本题难度:简单
3、填空题 (1)为了证明一水合氨是弱碱,甲、乙、丙三同学分别设计以下实验进行探究。
①甲同学用pH试纸测得室温下0.10 mol・L-1氨水pH为10,则认定一水合氨是弱电解质,理由是 。
②乙同学取10 mL 0.10 mol・L-1氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000 mL,再用pH试纸测出其pH为b,若要确认一水合氨是弱电解质,则a、b应满足的关系是 (用等式或不等式表示)。
③丙同学取出10 mL 0.10mol・L-1氨水,滴入2滴酚酞试液,显粉红色,再加入NH4Cl晶体少量,观察到的现象是 ,则证明―水合氨是弱电解质。
(2)向25 mL 0.10 mol・L-l的盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是 。
a.c(C1-)=c(NH4+)>c(H+)=c(OH-) b.c(C1-)>c(NH4+)=c(H+)>c(OH-)
c.c(NH4+)>c(OH-)>c(C1-)>c(H+) d.c(OH-)>c(NH4+)>c(H+)>c(C1-)
(3)常温下,0.10mol・L-l的NH4Cl溶液pH为5,则一水合氨的电离常数Kb= 。
参考答案:(1) ①如果氨水是强碱,0.10mol?L-1氨水pH为1
本题解析:
试题分析:(1)若证明一水合氨是弱碱,需从以下几个角度考虑:a、看电离程度b、看是否存在电离平衡c、测盐溶液的pH。 ①甲同学用pH试纸测得室温下0.10 mol・L-1氨水pH为10,则认定一水合氨是弱电解质,理由是如果氨水是强碱,0.10mol?L-1氨水pH为13,溶液的pH=10<13,所以一水合氨是弱碱;②若是强碱,稀释100倍,pH减小2个单位,由于一水合氨是弱碱,稀释的过程中,促进电离,c(OH-)变化的幅度变小,pH减小幅度小于2个单位,则有a-2<b,且b<a;答案为:(a-2)<b<a;③如果一水合氨是弱碱,则存在电离平衡NH3・H2O  NH4+ + OH-,向氨水中加入氯化铵后,铵离子浓度增大,平衡逆向移动,溶液中氢氧根离子浓度降低,溶液的碱性减弱,则溶液的颜色变浅;(2)向25 mL 0.10 mol・L-l的盐酸中滴加氨水至过量,a.氨水稍过量,混合液呈中性,c(C1-)=c(NH4+)>c(H+)=c(OH-) ,正确;b.盐酸过量,溶液为盐酸和氯化铵的混合液,溶液显酸性,c(C1-)>c(NH4+)=c(H+)>c(OH-),正确;c.氨水远远过量,溶液为氨水和氯化铵的混合液,一水合氨的电离程度大于铵离子的水解程度,溶液呈碱性,c(NH4+)>c(OH-)>c(C1-)>c(H+),正确;d.不可能出现c(OH-)>c(NH4+)>c(H+)>c(C1-),错误;选abc; (3)常温下,0.10mol・L-l的NH4Cl溶液pH为5,NH4+的水解常数Kh=[H+][NH3・H2O]/[NH4+]=10―9,水合氨的电离常数 NH4+ + OH-,向氨水中加入氯化铵后,铵离子浓度增大,平衡逆向移动,溶液中氢氧根离子浓度降低,溶液的碱性减弱,则溶液的颜色变浅;(2)向25 mL 0.10 mol・L-l的盐酸中滴加氨水至过量,a.氨水稍过量,混合液呈中性,c(C1-)=c(NH4+)>c(H+)=c(OH-) ,正确;b.盐酸过量,溶液为盐酸和氯化铵的混合液,溶液显酸性,c(C1-)>c(NH4+)=c(H+)>c(OH-),正确;c.氨水远远过量,溶液为氨水和氯化铵的混合液,一水合氨的电离程度大于铵离子的水解程度,溶液呈碱性,c(NH4+)>c(OH-)>c(C1-)>c(H+),正确;d.不可能出现c(OH-)>c(NH4+)>c(H+)>c(C1-),错误;选abc; (3)常温下,0.10mol・L-l的NH4Cl溶液pH为5,NH4+的水解常数Kh=[H+][NH3・H2O]/[NH4+]=10―9,水合氨的电离常数
Kb=[OH-][NH4+]/[NH3・H2O]=Kw/Kh=1×10―5。
考点:考查强弱电解质的比较、酸碱混合溶液中离子浓度大小比较及电离平衡常数计算。
本题难度:困难
4、选择题 两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是
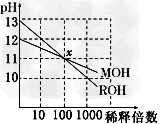
[????? ]
A、MOH是一种弱碱??????????????????
B、在x点,c(M+)=c(R+)
C、稀释前,c(ROH)=10?c(MOH)????
D、稀释前MOH溶液和ROH溶液中由水电离出的c(OH-)? 后者是前者的?10倍????
参考答案:CD
本题解析:
本题难度:一般
5、选择题 从下列现象可以判断某一元酸是强酸的是( )
A.加热该酸至沸腾也不分解
B.该酸溶液可与石灰石反应放出CO2
C.该酸溶液可以溶解Al(OH)3沉淀
D.该酸溶液浓度为0.1mol/L时pH=1
参考答案:A.弱酸也可以沸腾不分解,如:乙酸是弱酸,但它在440℃的高
本题解析:
本题难度:简单
|