微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关化学用语表达不正确的是[???? ]
A.氨气分子的电子式: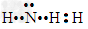
B.S2-的结构示意图: ??
??
C.CS2分子的结构式:S=C=S
D.苯分子的比例模型: ?
?
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列各项表述正确的是 [???? ]
A.羟基的电子式:
B.醛基官能团符号:-COH
C.铝离子结构示意图: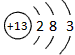
D.异丁烷的结构简式: CH3CH(CH3)CH3
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列有关叙述正确的是
A.氢键是一种特殊化学键,它广泛地存在于自然界中
B.在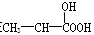 分子中含有1个手性C原子
分子中含有1个手性C原子
C.碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子。
D.含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大
参考答案:B
本题解析:
试题分析:氢键不是化学键,选项A不正确;如果饱和碳原子上连接的4个基团分别都不相等,则B中物质只有1个手性碳原子,B正确;单质碘是非极性分子,选项C不正确;含氧酸可用通式XOm(OH)n来表示,m值越大,则含氧酸的酸性越大,D不正确,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,贴近高考,侧重对学生基础知识的巩固和检验,同时结构对学生能力的培养,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于提高学生的应试能力。
本题难度:一般
4、填空题 已知元素A、B、C、D和E的原子序数依次增大。A、B、C、D四种元素核电荷数均小于20,A、B同主族;B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1;E是周期表中(除放射性元素外)第一电离能最小的元素。回答下列问题:
(1)写出下列元素的符号:A ??????、E???????。
(2)C元素的价电子排布图为:????????????????????????????;
该排布遵循的原理主要有:????????????????????????????????????????(答完整得分)。
(3)C、D元素形成的化合物主要有:??????????(填化学式,答完整得分);其中相对分子质量较小的分子为??????分子(填“极性”或“非极性”),该分子的空间构型为????????,中心原子的杂化方式是???????。
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为?????;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于?????形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中 和
和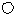 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的??(填序号),在该晶胞中阳离子的配位数为??。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的??(填序号),在该晶胞中阳离子的配位数为??。
参考答案:(1)B????? Cs??(2) 本题解析:
本题解析:
试题分析:(1)B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1,且原子序数依次递增,都小于20,所以B是硼或铝元素,由于A和B是同主族的,且A的原子序数最小,所以B是Al,A是B,则C是P,D是Cl。E是周期表中(除放射性元素外)第一电离能最小的元素,由于金属性越强,第一电离能越小,所以E是Cs。
(2)根据构造原理可知,P元素的价电子排布图为 本题难度:一般
本题难度:一般
5、填空题 太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。
(1)亚铜离子(Cu+)基态时的价电子排布式表示为??????????????????。
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为????????????(用元素符号表示)。
(3)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质。
①[B(OH)4]-中B的原子杂化类型为?????????????????????;
②不考虑空间构型,[B(OH)4]-的结构可用示意图表示为????????????????????。
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得右图所示的金刚砂(SiC)结构;若在晶体硅所有Si―Si键中插入O原子即得SiO2晶体。
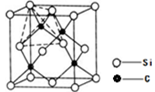
①在SiC中,每个C原子周围最近的C原子数目为???????????????????;
②判断a. SiO2,b.干冰,c.冰3种晶体的熔点从小到大的顺序是????????(填序号)。
参考答案:(12分)
(1)3d10 (2分)??(2)Br&
本题解析:
试题分析:
(1)亚铜离子是由铜原子失去了一个电子得到的,所以有28个电子,所以为3d10;
(2)由于AS的外围电子排布式为4S24P3每个轨道电子处于半充满状态,能量比较低,比较稳定,失去电子较困难。
(3)①根据价层电子互斥理论,[B(OH)4]-中B中价电子数为(3+4+1)/2=4,所以应该是SP3杂化;
②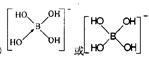 91eXaM.org
91eXaM.org