?
�ο��𰸣���5�֣�
���ӻ�����
�¶Ե��Ӷ���
VSE
������������ݼ۲���ӶԻ������ۿ�֪������֪̼ԭ�Ӻ��еŶԵ��Ӷ����ǣ�4��1��4����2��0�����Լ�����ӵĹ��������������Σ�����̼ԭ����sp3�ӻ���BeCl2��Beԭ�Ӻ��еŶԵ��Ӷ����ǣ�2��1��2����2��0�������ֱ���ͽṹ������sp�ӻ���SO2����ԭ�Ӻ��еŶԵ��Ӷ����ǣ�6��2��2����2��1����SO2��V�νṹ����sp2�ӻ���CH3+��̼ԭ�Ӻ��еŶԵ��Ӷ����ǣ�4�D1�D1��3����2��0�������ƽ�������νṹ������sp2�ӻ���SO42������ԭ�Ӻ��еŶԵ��Ӷ����ǣ�6��2��2��4����2��0����������������
�����Ѷȣ�һ��
3������� ��14�֣���Ԫ�ؿ����γɶ��ֻ�����ش��������⣺
��1����̬��ԭ�ӵļ۵����Ų�ʽ��_________________��
��2��C��N��O����Ԫ�ص�һ�����ܴӴ�С��˳����____________��
��3����(N2H4)���ӿ���ΪNH3�����е�һ����ԭ�ӱ���NH2��������ȡ���γɵ���һ�ֵ����⻯�
��NH3���ӵĿռ乹����_______________��N2H4�����е�ԭ�ӹ�����ӻ�������___________��
���¿��������ȼ�ϣ�ȼ��ʱ�����ķ�Ӧ�ǣ�
N2O4(l)��2N2H4(l)===3N2(g)��4H2O(g)???��H=��1038.7kJ��mol��1
���÷�Ӧ����4mol N��H�����ѣ����γɵĦм���________mol��
�����������ᷴӦ����N2H6SO4��N2H6SO4�����������������ͬ����N2H6SO4�ľ����ڲ�����__________(����)
a. ���Ӽ�???? b. ���ۼ�???? c. ��λ��??? d. ���»���
��4��ͼ1��ʾij�ֺ����л�������Ľṹ���������4����ԭ�ӷֱ�λ�����������4�����㣨��ͼ2���������ڴ��ڿ�ǻ����Ƕ��ij���ӻ���Ӳ��γ�4���������ʶ��

���з��ӻ������У��ܱ����л�������ʶ�����_________�����ţ���
a. CF4????? b. CH4????? c. NH4��???? d. H2O
�ο��𰸣���1��2s22p3?????��2��N��O��C
��3��
�����������1�����ݹ���ԭ����д����̬��ԭ�ӵļ۵����Ų�ʽ��2s22p3��
��2���ǽ�����Խǿ����һ������Խ������N�е�2p�ǰ�������ȶ���ǿ�����Ե�һ�����ܴ���O�ģ�˳��ΪN��O��C��
��3����NH3����������ԭ�Ӻ���1�Թ¶Ե��ӣ������������νṹ��NH3�е�ԭ�ӹ�����ӻ�������sp3������(N2H4)���ӿ���ΪNH3�����е�һ����ԭ�ӱ���NH2��������ȡ���γɵģ�����N2H4�����е�ԭ�ӹ�����ӻ�������sp3�������H2O��H2O2��O���ӻ����Ͷ���sp3�ĵ�����һ���ġ��ڸ��ݷ�Ӧʽ��֪������
�����Ѷȣ�һ��
4������� ��1����ѧ��ͨ��X�����Ʋ���ṹʾ��ͼ�ɼ�ʾ���£�ͼ�����߱�ʾ���������ֱ�Ϊ????????????????????????
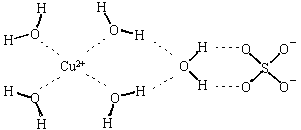
��2��������ͭ��Һ����εμӰ�ˮ���������ȳ�����ɫ����������ܽ��γ�����ɫ����Һ��д������ɫ�����ܽ�����ӷ���ʽ��????????????????????????????????????��
��3��SiCl4��SO42һ��Ϊ�ȵ����壬Ԥ��SO42һ�Ŀռ乹��Ϊ??????????????????????????????
�ο��𰸣���1�����??��λ�� ��6�֣�
��2��Cu(OH)2��
���������
��1����ԭ�ӵ縺�Խϴ�����ԭ�Ӽ��γ����������ԭ��ͭ�����пչ������ԭ���ṩ�µ��Ӷԣ�Cu2����O�γ���λ����
��2��Cu(OH)2��4NH3��H2O����Cu(NH3)4��2����2OH����4H2O
��3��SiCl4��SO42һ��Ϊ�ȵ����壬SiCl4����ԭ��Si����sp3�ӻ����ռ乹����������,�ȵ�����ṹ���ƣ�Ԥ��SO42һ�Ŀռ乹���������塣
�����Ѷȣ�һ��
5������� д���������ʣ�
���ǻ��ĵ���ʽ______
��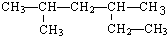 ������______ ������______
��1-�����Ĵ�������Cu��O2������ʽ______��
�ܱ�����Һ�еμ�Ũ��ˮ��Һ������ɫ�����ķ���ʽ______��
�ο��𰸣�����ԭ������ԭ��ͨ��һ�Թ��õ��Ӷ����ӣ��ǻ��е���ԭ�Ӻ���һ
���������
�����Ѷȣ�һ��
|