��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��ʾ��ȷ���ǣ�???��
A��AgNO3��Һ�м���Cu��Cu + Ag+ = Cu2+ + Ag
B��NaHSO4��Һ��Ba��OH��2��Һ��Ӧ�����ԣ�H++SO42��+Ba2++OH��=BaSO4��+H2O
C��������Һ�ε�����ʯ̨���������ݲ�����2H+ + CaCO3 = CO2��+ Ca2+ + H2O
D������������ʵ���Ũ�ȵ�NaHCO3��Ba(OH)2��Һ��ϣ�
HCO3- + Ba2+ + OH- = BaCO3��+ H2O
�ο��𰸣�D
���������
���������A��û����ƽ������B�Ӧ�����ԣ�H+��OH?��ȫ��Ӧ�����ߵ�ϵ��Ӧ����2����B�������Ϊ���ᣬ���ܲ��������ʽ��C�����NaHCO3��Ba(OH)2�����ʵ�����Ӧ��Ba(OH)2��Ӧ1��OH?����D����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ���и���Ӧ�����ӷ���ʽ�У���ȷ����
A����������Һ�м�������İ�ˮ��Al3++3OH- ==Al(OH) 3
B��ͭ���Ȼ�����Һ��Ӧ��Cu + Fe3+ ="=" Cu2+ + Fe2+
C��NaHCO3��Һ��NaHSO4��Һ��Ӧ��HCO3- + H+= H2O + CO2 ��
D��������,Cl2��ˮ�ķ�Ӧ��Cl2 + H2O = 2H+ + Cl- + ClO-
�ο��𰸣�C
���������A����ˮΪ���ᣬ���ܲ�Ϊ������ʽ���ų�
B����ɲ��غ㣺Cu + 2Fe3+ ="=" Cu2+ + 2Fe2+������ȷ
C����ȷ
D������HClOΪ���ᣬ���ܲ�Ϊ������ʽ������ȷ
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A������������̼ͨ�롰ˮ�������У�CO2+SiO32-+H2O�TCO32-+H2SiO3��
B��̼������ڴ��CaCO3+2H+�TCa2++H2O+CO2��
C�������ռ���Һ��2Al+2OH-+2H2O=2AlO2-+3H2��
D��AlCl3��Һ�м��������ˮ��Al3++4OH-=AlO2-+2H2O
�ο��𰸣�A������������̼��ӦӦ����HCO3-����ȷ�����ӷ���ʽΪ2C
���������
�����Ѷȣ���
4��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A��Fe2O3���ڹ����������Һ�У�Fe2O3 + 6H+ + 2I-=2Fe2+ + I2 +3H2O
B��������NaOH��Һ��Ӧ��2Al + 2OH��=2AlO2��+ H2��
C��5.6 g Fe��200 mL 2.0 mol/L HNO3��Һ��ַ�Ӧ��3Fe + 2NO3-+ 8H+��3Fe2+ + 2NO�� + 4H2O
D��̼�������Һ��������NaOH��Һ��Ϻ���ȣ�NH4����OH�� NH3����H2O
NH3����H2O
�ο��𰸣�A
���������
���������A��Fe2O3���ڹ����������Һ�У�Fe2O3 + 6H+ + 2I-=2Fe2+ + I2 +3H2O����ȷ��B��������NaOH��Һ��Ӧ��2Al + 2OH��=2AlO2��+ H2������ʧ������Ŀ����ȣ�����C��5.6 g Fe��200 mL 2.0 mol/L HNO3��Һ��ַ�Ӧ�����ӷ���ʽӦΪ��Fe + NO3-+ 4H+��Fe3+ + NO�� + 2H2O�����ﲻ�ԣ�����D��̼�������Һ������NaOH��Һ��Ϻ���ȣ�NH4����OH�� �����Ѷȣ�һ��
�����Ѷȣ�һ��
5������� A��B��C��D��E��F��G�������ʼ������ͼ��ʾ��ת����ϵ������A��B��D��G����ͬ��Ԫ�ء�
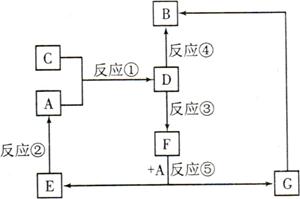
��֪��
AΪ�������ʣ�BΪ���ɫ���壬EΪ�ܶ���С�����壬GΪdz��ɫ����Һ��
D��ˮ��ҺΪ��ɫ��Һ��������������Һ��Ӧ���ɲ�����ϡ����İ�ɫ������
��ˮ��Һ��D�ܽ�ij����������ΪF��F�Ǻ�������Ԫ�صĻ����
��ش��������⣺
��1������C���ʵ�Ԫ�������ڱ��е�λ����?????���ڶ���������Ԫ���У���Ԫ����������Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳����?????????(��Ԫ�ط��ű�ʾ)��
��2��D��ˮ��Һ��???�ԣ��������ӷ���ʽ����ԭ��?????????????��
��3��������Ӧ�������û���Ӧ����?????(�����)��
��4����Ӧ��(��D��ij������������ΪF)�����ӷ���ʽ��???????????????��
��5��������C��������ʵ�顣��֪������Ӧ�����У�ÿ����0.1mol KI��ת�Ƶĵ�����ԼΪ3.612��1023�����밴��Ҫ����գ�
ʵ�鲽��
| ʵ������
| д���ӷ���ʽ
|
����������ͨ�����KI��Һ
| ��Һ������?????ɫ
| ?
|
����ͨ������
| ��Һ�����ɫ
| ?
?
�ο��𰸣���1���������� �ڢ� A�� �� S > Cl >
���������
���������������֪��BΪ���ɫ���壬BΪFe(OH)3, EΪ�ܶ���С�����壬EΪH2��GΪdz��ɫ����Һ����GΪFe2+��Һ��D��ˮ��ҺΪ��ɫ��Һ��������������Һ��Ӧ���ɲ�����ϡ����İ�ɫ��������DΪFeCl3 ���ɷ�Ӧ����֪AΪFe��CΪCl2
��1������C���ʵ�Ԫ������Ԫ�����ڱ��е�λ���ǵ������� �ڢ� A�� ������ԭ�Ӱ뾶�Ĵ�С�������ؿ�֪����Ԫ����������Ԫ��S��F��ԭ�Ӱ뾶�Ĵ�С��ϵ��S > Cl > F
��2��FeCl3��Һ�����ԣ�����ΪFe3+ˮ���Ե�ʣ�ˮ�����
�����Ѷȣ�һ��
|