��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и�������������Һ�д����������
A��Na+��Mg2+��Cl-��OH-
B��H+��Ca2+��CO32-��NO3-
C��Cu2+��K+��SO42����NO3-
D��Na+��H+��OH-��Ca2+
�ο��𰸣�C
���������
���������A��þ���Ӻ����������ӷ�Ӧ����������þ���������ܴ������棬����B�������Ӻ�̼������ӷ�Ӧ����ˮ�Ͷ�����̼�����ܴ������棬����C���������Ӷ����������ӷ�Ӧ�����Դ������棬��ȷ��D�������Ӻ����������ӷ�Ӧ����ˮ�����ܴ������棬����ѡC��
���㣺�������Ӵ���������ж�
�����Ѷȣ�һ��
2��ѡ���� ij������Һ��ֻ��Na����CH3COO����H����OH���������ӡ�������������ȷ����(??? )
A��pH��11��NaOH��Һ��pH��3�Ĵ�����Һ�������ϣ�����ʯ����Һ����ɫ
B������Һ�ɵ����ʵ���Ũ�ȡ��������NaOH��Һ��CH3COOH��Һ��϶���
C����NaOH��Һ�м���һ������CH3COOH��Һ��ֻ�е���Һ������Ũ�����㣺
c(Na��)��c(CH3COO��)��c(OH��)��c(H��)ʱ���ŷ������⡣
D������������ˮ��c(CH3COO��)һ������c(Na��)��c(NH4��)֮��
�ο��𰸣�B
�������������Ҫǿ���������������ԡ����ó���c(OH��)��c(H��)���ٸ��ݵ���غ��Ƴ�(Na��)��c(CH3COO��)��
A��ǡ������n(OH��)=n(H��),����ͼ��ѵ�������ġ�H����OH��ǡ����ȫ�кͣ��������ڴ��������ᣬ������δ���룬������ʣ�࣬�ʻ�Ϻ���Һ�����ԡ�
B���ǵ����ʵ���Ũ�ȡ��������NaOH��Һ��CH3COOH��Һ��ϣ���ǡ���к�ת����ΪCH3COONa��Һ������ǿ����������Һ���ʳʼ��ԣ��Ϻ����⡣
C����c(Na��)��c(CH3COO��)��c(OH��)��c(H��)ʱ������
�����Ѷȣ���
3��ѡ���� �ڸ����������£����и��������ܴ����������???????????�� ????��
A���μӷ�̪��Һ�Ժ�ɫ����Һ Fe3+��NH4+��Cl-��SCN-
B��ˮ���������c(H��)=10-13mol/L����Һ K+��HCO3-��Br-��Ba2������
C��pH=12����Һ K+��ClO-��NO3-��H+
D��pH=1����Һ Cu2+��Na+��Mg2+��Cl-
�ο��𰸣�D
���������
���������A����Fe3+��SCN-���ܴ������棬B����ˮ���������c(H��)=10-13mol/L����Һ��������Ի��ǿ���ԣ�HCO3-���ܴ������棬C����pH=12����Һ�Ǽ�����Һ��H+���ܴ������档��ѡD��
���������Ӳ��ܴ��������һ������ǣ���1���ܷ������ֽⷴӦ������֮�䣨�����ɳ��������壬ˮ�����ᡢ������ѵ������ʣ�����2�������������������֮�䣨�磺Ca2+�� SO42-��Ag+�� SO42-������3������ȫˮ�������֮�䣬���Ԫ����������ε����������ӣ��磺Al3+�� Fe3
�����Ѷȣ�һ��
4������� ��15�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4]�D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ������»�ԭ���������Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸���
�����������£�
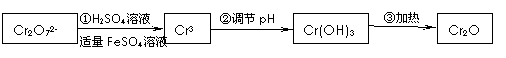
�й�������ȫ������pH���±���
�����
| Fe2+
| Fe3+
| Cr3+
|
��ȫ����Ϊ��Ӧ���������pH
| 9.0
| 3.2
| 5.6
��1��д��Cr2O72�D��FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ���� ��������������������
��2����ԭ+6�۸�����ѡ�����µ������������Լ�������ţ���
A���������������� B����м������ ����C����ʯ�ҡ����� ������D������������
��3���ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�����������������
�ڲ������е���pHӦ��2�ν��У���1��Ӧ�ȵ�����Һ��pH��ΧԼ��������������ţ���ѣ���2��Ӧ������Һ��pH��ΧԼ��������������ţ����
A��3��4������ ��B��6��8������ ����C��10��11������������ D��12��14
���ڵ�����Һ������Լ�Ϊ����������������������������ţ���
A��Na2O2����������B��Ba(OH)2��������C��Ca(OH)2���������� D��NaOH
�ο��𰸣���15�֣���1��Cr2O72�D+ 6 Fe2+ + 14H+
�����������
�����Ѷȣ�һ��
5��ѡ���� 25��ʱ�����и���������ָ����Һ��һ���ܴ����������
A������ʯ����Һ����ɫ����Һ�У�K+��Na-��HSO3-��ClO-
B��0.1mol?L-l��Fe(NO3)2��Һ�У�Na+��H+��SCN-��I-
C��0.1mol?L-l��NaAlO2��Һ�У�K+��H+��NO3-��SO42-
D����ˮ���������c(H+)=1��10-13mol?L-l����Һ�У�Na+��Ba2+��NO3-��Cl-
�ο��𰸣�D
���������
���������A������ʯ����Һ����ɫ����Һ�ʼ��ԣ�������Һ��OH����HSO3-��Ӧ�������������ˮ��HSO3-��ClO-����������ԭ��Ӧ����������������ӣ����ܴ������棬����B��0.1mol?L-l��Fe(NO3)2��Һ��H+��NO3-��I-����������ԭ��Ӧ�����ܴ������棬����C��0.1mol?L-l��NaAlO2��Һ�У�H+��AlO2����ˮ��Ӧ���������������������ܴ������棬����D����������£��������Ӽ䲻��Ӧ���ܴ������棬��ȷ��
���㣺�������ӷ�Ӧ�����ӹ������⡣
�����Ѷȣ�һ��
|