2.40
��1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2mol��L��1��CO��ƽ��Ũ��Ϊ_____________��
��2����Ӧ���е�a__________0������ڡ�С�ڡ����ڣ���
��3��700�淴Ӧ�ٴﵽƽ�⣬Ҫʹ�ø�ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ��__________������ţ�
A.��С��Ӧ�����??????????????????????????? B.ͨ��CO2
C.�����¶ȵ�900��?????????????????? D.ʹ�ú��ʵĴ���
��4������ͼ����Ϸ�Ӧ�ٵ���___________������ţ���ͼ��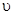 �����ʡ� �����ʡ� Ϊ�������CO������TΪ�¶���T1��T2�� Ϊ�������CO������TΪ�¶���T1��T2��

��5���ɷ�Ӧ�ٺ͢ڿ���ã���Ӧ2Fe��s��+O2��g��=2FeO��s���ġ�H=__________��
�ο��𰸣���1��1mol��L��1��2�֣�??��2�����ڣ�2�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ��֪��I2(aq)��I��(aq) I3��(aq)��ijI2����KI�����Һ�У�c(I3��)���¶ȣ�T���Ĺ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵���У���ȷ���� I3��(aq)��ijI2����KI�����Һ�У�c(I3��)���¶ȣ�T���Ĺ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵���У���ȷ����
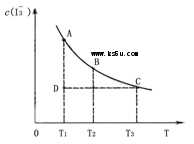
A����Ӧ I2(aq)��I��(aq)  I3��(aq)�ġ�H��0 I3��(aq)�ġ�H��0
B��״̬A��c(I2)��״̬D��С
C��A���Ӧ�ķ�Ӧ���ʴ���C���Ӧ�ķ�Ӧ����
D�������������䣬����Һ�м���KI���壬ƽ����C���ƶ���D��
�ο��𰸣�B
���������
��ȷ�𰸣�B
A������ȷ����ͼ�ó����¶����ߣ�I3�DŨ�ȱ�С��ƽ�������ƶ�����HС��0��
B����ȷ��
C������ȷ��A���Ӧ�ķ�Ӧ���ʲ���C���Ӧ�ķ�Ӧ���ʣ�A���¶ȵͣ�
D������ȷ�������������䣬����Һ�м���KI���壬���������ƶ���ƽ����C���ƶ���A�㣻
�����Ѷȣ�һ��
3��ѡ���� ��H2��N2�������Ϊ3��1����һʢ�д������ܱ������У���һ�������·�Ӧ�ﵽƽ��״̬������˵����ȷ���ǣ�???��
A��ƽ�������У�H2��N2�������һ����3��1
B��ƽ�������У�H2��NH3�������һ����1��1
C��ƽ�������У�N2��NH3�������һ����1��2
D��ƽ�������У�H2��N2��NH3�������һ����3��1��2
�ο��𰸣�A
����������÷�ӦͶ�����뻯ѧ��������ȣ����ʣ����֮��Ҳ�뻯ѧ��������ȡ�
�����Ѷȣ���
4��ѡ���� ��10L�ܱ������У�1moLA��3moLB��һ�������·�Ӧ��
A��g��+xB��g�� 2C��g������2min��Ӧ�ﵽƽ��ʱ����û�����干3.4moL������0.4moLC�� �����м���������ȷ���ǣ�???�� 2C��g������2min��Ӧ�ﵽƽ��ʱ����û�����干3.4moL������0.4moLC�� �����м���������ȷ���ǣ�???��
A��ƽ��ʱ�����ʵ���֮��A�UB�UC=2�U11�U4
B��xֵ����4
C��A��ת����Ϊ20%
D��ƽ��ʱB��ƽ����Ӧ����Ϊ0.04moL����L��min��
�ο��𰸣�A
���������
�����������Ӧ�ﵽƽ��ʱ���������Ϊ3.4moL������0.4moLC�� �������ĵ�AΪ0.2mol�����ĵ�BΪ3-[3.4-(1-0.2+0.4)]=0.8������=������xΪ4��B��ȷ��A��ת����=0.2/1��100%=20%����C��ȷ��ƽ��ʱB��ƽ����Ӧ����=0.8/10/2=0.04moL����L��min������D��ȷ��ƽ��ʱ��A�����ʵ���Ϊ0.8mol��B�����ʵ���Ϊ3.4-(1-0.2+0.4)=2.2mol������ƽ��ʱ���ʵ���֮��A�UB�UC=0.8��2.2��0.4=4��11��2����A����ȷ��Ϊ����Ĵ𰸡�
���������⿼���˻�ѧƽ���֪ʶ�㣬�ÿ����Ǹ߿�������ص㣬�����漰�˻�ѧƽ��ļ��㣬�Ѷ����С�
�����Ѷȣ�һ��
5������� ��16�֣�̼���仯��������������������������ء���ش��������⣺
��1���ڻ������������У�����CO�Ĵ��ڻ���������ж���Ϊ�˷�ֹ�����ж�������SO2��CO����SO2����ԭΪS��
��֪�� C(s)+ ��g��=CO��g����H1=-126��4kJ/mol????????�� ��g��=CO��g����H1=-126��4kJ/mol????????��
C(s)+O2��g��=CO2��g��? ��H2= ��393��5kJ��mol��1???????��
?????????????????S(s)+O2��g��=SO2��g��???��H3= ��296��8kJ��mol��1?????????��
��SO2����CO���Ȼ�ѧ��Ӧ����ʽ��??????????????????????????????
��2��CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)+2H2(g) CH3OH(g)�� CH3OH(g)��
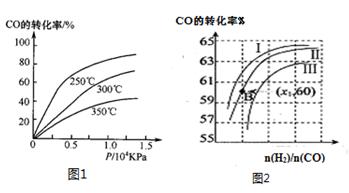
��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ1��ʾ���÷�Ӧ��H?????0���>���� <������
ͼ2��ʾCO��ת��������ʼͶ�ϱ�[ n(H2)/n(CO)]���¶ȵı仯��ϵ������I��II��III��Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2��K3����K1��K2��K3�Ĵ�С��ϵΪ?????????�����B(X1,60)��������ת����Ϊ40%����x1=????????��
���ں����ܱ������ﰴ�����Ϊ1:2����һ����̼��������һ�������·�Ӧ�ﵽƽ��״̬�����ı䷴Ӧ��ijһ�����������б仯��˵��ƽ��һ��������Ӧ�����ƶ�����??????������ţ���
A������Ӧ������������С
B���淴Ӧ������������С
C����ѧƽ�ⳣ��Kֵ����
D����Ӧ�������ٷֺ�������
E�� ���������ܶ�����
��һ�������£���2molCO��2molH2�����ݻ�Ϊ2L�̶����ܱ������з���������Ӧ����Ӧ�ﵽƽ��ʱCO��H2���֮��Ϊ2��1����ƽ�ⳣ��K��??????????????��
��3�������о����֣��ø�Ĥ��ⷨ���Դ�����Ũ����ȩ��ˮ��
ԭ����ʹ�ö��Ե缫��⣬��ȩ�ֱ�����������ת��Ϊ�Ҵ������ᣬ
�ܷ�ӦΪ:2CH3CHO+H2O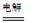 CH3CHOH+CH3CHOOH�� CH3CHOH+CH3CHOOH��
ʵ�����У���һ��Ũ�ȵ���ȩ-Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ��?�������̣���װ��ʾ��ͼ��ͼ��ʾ��
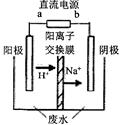
�ٵ������У��������ֱ�����������Ҵ��⣬��������ɫ���壬�����缫��Ӧ�ֱ�Ϊ��
4OH��-4e���TO2��+2H2O��???????????????????????????????????��
����ʵ�ʹ��մ��������У���������ȩ��ȥ���ʿɴ�60%�������������ֱ�ע��1m3��ȩ�ĺ���Ϊ300mg/L�ķ�ˮ���ɵõ��Ҵ�????????kg(����������2λС����
�ο��𰸣���16�֣�
��1�� SO2��g��+2CO��g��=S(s
���������
�����������1�����ݸ�˹���ɵã�Ŀ�귽��ʽ=�ڡ�2-�١�2-�ۣ���H=����393��5kJ��mol��1����2-��-126��4kJ/mol����2-����296��8kJ��mol��1��=-237��4kJ��mol��1�����������Ȼ�ѧ����ʽΪSO2��g��+2CO��g��=S(s)+2CO2��g��? ��H=-237��4kJ��mol��1��
��2������ͼ1��֪���¶�����CO��ת���ʽ��ͣ�˵�������¶ȣ�ƽ�������ƶ��������Ƿ��ȷ�Ӧ����H<0��n(H2)/n(CO)һ��ʱ��CO��ת���ʢ�>��>��ת���ʸߵ�ƽ�ⳣ��������K1��K2��K3�Ĵ�С��ϵΪK1>K2>K3���B(X1,60)��������ת����Ϊ40%��CO��ת������60%����B��ʱCO��H2�����ʵ����ֱ���m��n���ɵ�60%m=40%n/2������n/m=3,��x1=3��
��A������Ӧ��Ũ�ȣ�����Ӧ������������С��˵��ƽ�������ƶ�����ȷ��B������������Ũ�ȣ��淴Ӧ������������С��˵��ƽ�������ƶ�������C�������¶ȣ�Kֵ����˵��������Ũ������Ӧ��Ũ�ȼ�С��ƽ�������ƶ�����ȷ��D����Сѹǿ��ƽ�������ƶ�����Ӧ�������ٷֺ���������E����������ʱ���������ܶ�����˵�������������������ӣ������Ƿ�Ӧ��Ҳ�����������ƽ���ƶ�����ȷ��������ѡAC��
����ƽ��ʱCO��Ũ����x����������Ũ����2x-1�����ɼ״���Ũ����1-x����������ã�x/(2x-1)=2:1,x=2/3mol /L,����K=(1-x)/x��(2x-1)2=4��5 L2��mol-2
��3������������������Ӧ����ȩ������Ϊ���ᣬ���������ӱ�����Ϊ������������������ԭ��Ӧ����ȩ����ԭΪ�Ҵ���ͬʱ�����ӱ���ԭΪ���������������缫��Ӧʽ�����������⣬����CH3CHO��2e��+H2O�TCH3COOH+2H+
��������Ӧ��CH3CHO+2e��+2H+=CH3CH2OH������ע��1m3��ȩ�ĺ���Ϊ300mg/L�ķ�ˮ����������ȩ��ȥ���ʿɴ�60%�������Ҵ���������1000L��300mg/L��60%��10-3g/mg��44g/mol��46g/mol=188��2g=0.19kg��
�����Ѷȣ�һ��
|