微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某学生鉴定甲盐的发如图所示:

下列结论正确的是( )
A.甲中一定有Fe3+
B.丙中一定有Fe3+
C.乙为AgI沉淀
D.甲一定为FeBr2溶液
参考答案:A.丙中含有Fe3+,可由Fe2+被氧化生成,不一定含有Fe
本题解析:
本题难度:一般
2、实验题 化学活动课上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性良好).观察现象,回答下列问题:
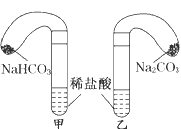
(1)各组反应开始时,________装置中的气球体积先变大,原因是___________________,该装置中反应的离子方程式是___________________________________________。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
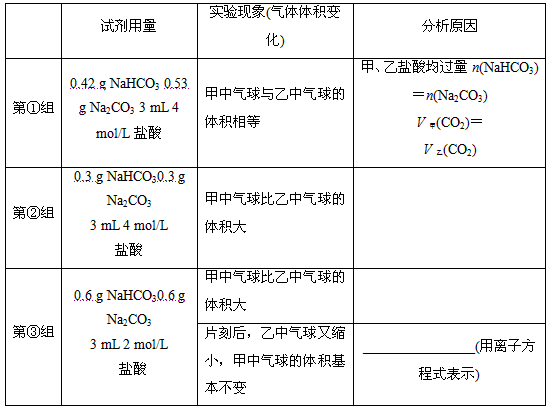
参考答案:
(1)甲因为NaHCO3与盐酸反应的速率大于Na2CO
本题解析:
本题难度:一般
3、简答题 由A和B两种正盐组成的混合物,进行了下列实验:
试判断,A、B分别是A______;B______.
写出实验过程中加水时发生反应的离子方程式:______.
参考答案:过滤后所得无色溶液加入硝酸钡溶液可得硫酸钡沉淀和硝酸钾溶液,
本题解析:
本题难度:一般
4、实验题 (10分)实验室有CuO和铜粉的混合物。要测定该样品(已称得其质量为m g)中氧化铜的质量分数。用下图所示仪器装置制取H2,再用H2还原CuO,最后根据样品质量的减少和无水CaCl2质量的增加来测定样品中氧化铜的质量分数。
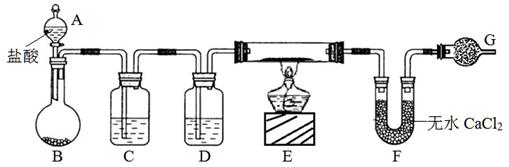
请回答:
(1)仪器中装入的试剂:D?????????????。
(2)操作“①打开A的活塞”和“②点燃E处酒精灯”应该先进行的是???(填序号),在这两步操作之间还应进行的操作是:????????????????????????????。
(3)若实验中有部分CuO被还原为红色的Cu2O,对实验的影响为_____(偏大、偏小、无影响)。
(4)若测得的原质量为a g的硬质玻璃管(E),反应后质量变为b g;U型管实验后质量增加n g,由以上数据可以列出计算氧化铜质量分数的两个不同计算式:
计算式1:???????????????;计算式2:????????????????????。
参考答案:(1)浓硫酸(1分)
(2)①(1分)收集G处的气体检
本题解析:(1)由于生成的氢气中含有水蒸气,会干扰后面的实验,所以D中的盛放的应该是浓硫酸,用来除去水蒸气。
(2)由于装置中含有空气,所以应该首先生成氢气,将装置中的空气排尽。氢气是可燃性气体,再点燃之前,需要收集G处的气体检验纯度。
(3)若实验中有部分CuO被还原为红色的Cu2O,则生成的水就减少,因此氧化铜的质量分数就减少。
(4)根据方程式H2+CuO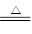 Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是
Cu+H2O可知,固体减少的质量就是氧化铜中氧原子的质量,所以氧化铜的质量是 ,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是
,所以氧化铜的质量分数是5(a-b)/m;生成水的质量是ng,则氧化铜的质量是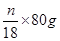 ,所以氧化铜的质量分数是40n/9m。
,所以氧化铜的质量分数是40n/9m。
本题难度:一般
5、选择题 下列实验操作与预期实验目的或所得实验结论一致的是
选项
| 实验操作
| 实验目的或结论
|
A
| 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤
| 除去MgCl2溶液中少量的FeCl3
|
B
| 向某溶液中加入BaCl2溶液生成白色沉淀,继续加稀硝酸沉淀不消失
| 证明溶液中含SO42-
|
C
| 向某溶液中加入稀盐酸,放出无色无味的气体,将气体通入澄清石灰水,石灰水变浑浊
| 证明该溶液中存在CO32-
|
D
| 向0.1mol/LFe SO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色
| 证明Fe2+具有氧化性
参考答案:A
本题解析:略
本题难度:一般
|