微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 合理使用材料,改善人类生活。
① 钢铁是人类生产和生活中非常重要的材料,但每年因锈蚀而损失的数量十分惊人。金属腐蚀分为化学腐蚀和电化学腐蚀,两者的微观本质都是发生????的过程。为防止轮船船体在海水中被腐蚀,一般在船身连接????(选填“锌块”或“铜块”)。
② 在普通玻璃制造过程中,碳酸钙与二氧化硅在高温下发生反应的化学方程式是
??????。橡胶是制造轮胎的重要原料,天然橡胶通过硫化措施,使它的分子转化为????结构,从而增大橡胶的强度。
参考答案:① 金属原子失去电子??锌块??
②? CaCO3 +
本题解析:
试题分析:①金属腐蚀的本质是金属失电子,被氧化的过程;为防止轮船船体在海水中被腐蚀,一般在船身连接比铁活泼的锌块,锌被腐蚀,从而保护铁;
②碳酸钙与二氧化硅在高温下发生反应生成硅酸钙和二氧化碳,化学方程式为CaCO3 + SiO2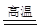 CaSiO3 + CO2↑;天然橡胶通过硫化处理,使它的分子转化为体
CaSiO3 + CO2↑;天然橡胶通过硫化处理,使它的分子转化为体
本题难度:一般
2、选择题 下列有关金属腐蚀与防护的说法正确的是
A.金属的电化腐蚀和化学腐蚀本质相同,但电化腐蚀伴有电流产生
B.钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气最终转化为铁锈
C.钢铁发生析氢腐蚀时,正极发生的电极反应为:Fe-2e-?Fe2+
D.埋在地下的钢管与电源正极连接可以减缓腐蚀
参考答案:A
本题解析:
试题分析:B不正确,发生吸氧腐蚀时,氧气在正极得到电子;铁作负极,负极发生的电极反应为:Fe-2e-?Fe2+,C不正确;铁和电源的正极相连,作阳极,失去电子,加速腐蚀,D不正确,答案选A。
点评:金属腐蚀主要是以电化学腐蚀为主。而在电化学腐蚀中,又主要以吸氧腐蚀为主。但不论是吸氧腐蚀,还是析氢腐蚀,金属都是作负极失去电子,据此可以进行有关判断,该题难度不大。
本题难度:一般
3、选择题 如图,缠上金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到在金属条表面的溶液出现粉红色。该金属条可能是??? ( )。
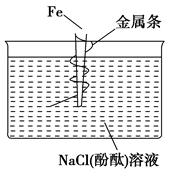
A.铜
B.镁
C.铝
D.锌
参考答案:A
本题解析:出现粉红色说明金属条附近产生了OH-,发生了吸氧腐蚀,金属条作正极,其活泼性比铁要差。
本题难度:简单
4、选择题 如图所示装置,两玻璃管中盛有含酚酞的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),若断开S1,接通S2,电流表的指针发生偏转。下列说法不正确的是
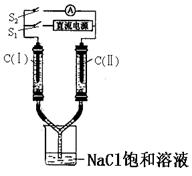
A.接通S1时,C(Ⅰ)的电极名称为阴极
B.接通S1时,直流电源的右边为正极
C.接通S2时,C(Ⅰ)电极反应式为H2-2e-+2OH-=2H2O
D.若将原来的电解质溶液换成含酚酞的MgCl2溶液,接通S1后现象相同
参考答案:D
本题解析:接通S1,形成了电解池。由C(Ⅰ)附近溶液变红,说明是H+放电,溶液呈碱性,为阴极,产生氢气。而C(Ⅱ)则是氯离子放电产生氯气。
一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,则形成了原电池。电池反应为:H2+Cl2=2HCl,其中氢气在负极失电子:电极反应式:H2-2e-+2OH-=2H2O,电子经导线流向正极:其反应式为:Cl2+2e-=2Cl-,氯气在正极得电子发生还原反应
若将原来的电解质溶液换成含酚酞的MgCl2溶液,接通S1后,C(Ⅰ)附近溶液变红, H+放电,溶液呈
本题难度:一般
5、选择题 有关下列电化学装置的说法中正确的是
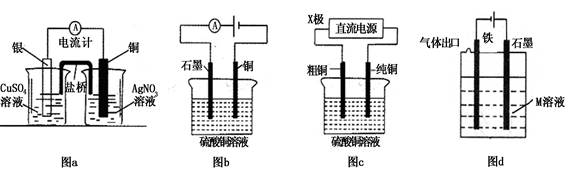
A.图a是原电池装置,可以实现化学能转化为电能
B.图b电解一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度
C.图c中的X极若为负极,则该装置可实现粗铜的精炼
D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
参考答案:B
本题解析:
试题分析:A、图a中铜电极应该插在硫酸铜溶液中,银电极应该插在硝酸银溶液中,A不正确;B、图b中石墨与电源的正极相连,做阳极,溶液中的OH-放电,生成氧气。铜电极和电源的负极相连,做阴极,溶液中的铜离子首先放电,生成铜。当铜离子完全放电后,溶液中的氢离子放电,生成氢气。所以如果铜离子还没有放电完全,则电解一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度,因为碳酸铜可以看作是CuO・CO2,Z正确;C、图c中如果X是负极,则应该连接纯铜,粗铜应该和电源的正极相连,C不正确;D、图d有
本题难度:一般