微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质的溶液加热蒸发至干、灼烧,所得固体的成分不相同的是()
A.FeCl2、FeCl3
B.Na2CO3、NaHCO3
C.NaAlO2、AlCl3
D.Mg(HCO3)2、MgCl2
参考答案:C
本题解析:A.FeCl2被氧化生成FeCl3,蒸发至干、灼烧,所得固体为Fe2O3。B所得固体为Na2CO3。C中NaAlO2溶液最终得到的是NaAlO2,AlCl3溶液最终得到的是Al2O3。D中Mg(HCO3)2、MgCl2溶液最终得到的都是MgO。
本题难度:简单
2、选择题 在0.1mol・L-1 的Na2CO3溶液中,下列关系正确的是
A.c(Na+)=2c(CO32-)
B.c(HCO3-)>c(H2CO3)
C.c(Na+)<[c(CO32-)+c(HCO3-)]
D.c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)
参考答案:B
本题解析:碳酸钠是强碱弱酸盐,CO32-水解显碱性,因此c(Na+)>2c(CO32-) ,A不正确。由于CO32-的第一步水解大于第二步水解,所以选项B正确。C不正确,不符合物料守恒,应该是c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]。D不正确,不符合质子守恒,应该是c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),答案选B。
本题难度:一般
3、实验题 (16分)(1)在中和滴定操作过程中,有以下各项因操作不当引起的实验误差,用“偏高”、“偏低”或“无影响”填空:
①滴定管用蒸馏水洗净后,未用已知浓度的标准溶液润洗,使滴定结果????????;
②锥形瓶用蒸馏水洗净后,又用待测溶液润洗,使滴定结果??????????;
③滴定管(装标准溶液)在滴定前尖嘴处有气泡,滴定终了无气泡,使滴定结果?????;
④滴定前平视,滴定终了俯视,使滴定结果??????????;
⑤用含Na2O杂质的NaOH固体来配制已知浓度的标准溶液,用于滴定未知浓度的盐酸,使测得盐酸的浓度???????????;
⑥洗涤锥形瓶时,误把稀食盐水当做蒸馏水,然后用锥形瓶装待测的盐酸,用NaOH标准溶液滴定时,对测得的结果???????????。
(2)已知H+(aq)+OH-(aq) = H2O(l)? ΔH= -57.3kJ・mol-1。用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
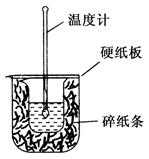
①从实验装置上看,图中尚缺少一种玻璃仪器是????????????????。
②大烧杯上如不盖硬纸板,求得的中和热数值????????(填“偏大”、“偏小”或“无影响”)。
③若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ・mol-1,其原因可能是:
???????????????????????????????????????????????????。
(3)分别设计化学实验,用最佳方法证明明矾溶于水时发生的下列变化(供选用的药品和仪器:明矾溶液、石蕊试液、酚酞试液、pH试纸、酒精灯):
①证明明矾发生了水解反应??????????????????????????????????????????????。
②证明其水解反应是一个吸热反应????????????????????????????????????????。
参考答案:(1)①偏高? ②偏高? ③偏高 ? ④偏低 ⑤偏低 ⑥
本题解析:
试题分析:(1)①未用已知浓度的标准液润洗滴定管,会导致标准液浓度偏小,反应所需标准液体积增大,从而导致最终结果偏高。②锥形瓶用待测液润洗,导致锥形瓶内残留有少量待测液,消耗的标准液的体积增大,从而导致最终结果偏高。③滴定前有气泡,滴定结束后无气泡,导致所测的体积增大,从而导致最终结果偏高。④滴定前平视,滴定终了俯视,使得计量体积减小,从而导致最终结果偏低。⑤因NaOH固体中含有杂质Na2O,使得配得的标准液浓度偏大,消耗的标准液的体积减小,从而导致最终结果偏小。⑥误用食盐水洗涤锥形瓶,对实验结果
本题难度:一般
4、选择题 下列方程式中属于水解反应的是
A.HCO3-+H2O  H3O++CO32-
H3O++CO32-
B.HCO3-+H2O  OH-+H2CO3
OH-+H2CO3
C.NH3+H2O  NH4++OH-
NH4++OH-
D.HCO3-+OH- =CO32-+H2O
参考答案:B
本题解析:
试题解析:A、该方程式为HCO3-电离的方程式,错误;B、HCO3-结合水电离产生的H+生成H2CO3,属于水解反应,正确;C、是氨气与水反应的方程式,错误;D、是H2CO3与OH-反应的方程式,错误,答案选B。
本题难度:一般
5、选择题 已知酸H2B在水溶液中存在下列关系:①H2B = H++HB―,②HB―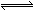 H++B2―,则下列说法中一定正确的是
H++B2―,则下列说法中一定正确的是
A.NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
B.Na2B溶液一定呈碱性,NaHB溶液可能呈酸性也可能呈碱性
C.NaHB水溶液中一定有:c(Na )+c(H
)+c(H )=c(HB
)=c(HB )+c(OH
)+c(OH )+c(B
)+c(B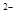 )
)
D.在Na2B溶液中一定有:c(OH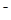 )=c(H
)=c(H )+c(HB
)+c(HB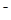 )
)
参考答案:AD
本题解析:
正确答案:AD
A.正确,NaHB不水解,溶液一定呈酸性,Na2B水解,溶液一定呈碱性
B.不正确;
C.不正确,NaHB水溶液中一定有:电荷守恒应为c(Na )+c(H
)+c(H 本题难度:一般
本题难度:一般