微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA是阿伏伽德罗常数的数值,下列说法正确的是
A.1molNa+离子含有的核外电子数为NA
B.1molCl2与足量的铁反应,转移的电子数为3NA
C.标准状况下,22.4L的CCl4中含有的CCl4分子数为NA
D.常温下,10LpH=13的NaOH溶液中含有的OH-离子数为NA
参考答案:D
本题解析:
试题分析:钠离子是10电子微粒,1molNa+离子含有的核外电子数为10NA,A不正确;氯气在反应中得到2个电子,所以1molCl2与足量的铁反应,转移的电子数为2NA,B不正确;标准状况下,四氯化碳是液态,不能适用于气体摩尔体积,C不正确;常温下,10LpH=13的NaOH溶液中含有的OH-离子的物质的量是10L×0.1mol/L=1mol,所以选项D正确,答案选D。
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的
本题难度:简单
2、选择题 质量相同的两种气体A、B,在同温、同压下,A的分子数比B多.下列说法正确的( )
A.A占的体积比B小
B.A的摩尔质量比B大
C.A的密度比B小
D.A的物质的量比B小
参考答案:质量相同的两种气体A、B,A的分子数比B多,根据N=nNA可
本题解析:
本题难度:一般
3、选择题 设NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA
B.1 mol硫酸钾中阴离子所带电荷数为NA
C.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA
D.常温下,0.1mol/L的NH4NO3溶液中氮原子数为0.2NA
参考答案:C
本题解析:
试题分析:虽然5.6L÷22.4L/mol=0.25mol,但是四氯化碳的物质的量不等于0.25mol,因为标准状况下四氯化碳是液体,液体摩尔体积不等于气体摩尔体积,故A错误;n(K2SO4)=1mol,K2SO4=2K++SO42ˉ,根据系数之比等于物质的量之比可知,n(阴离子)= n(K2SO4)=1mol,则N(阴离子)=NA,由于1个阴离子带2个负电荷,则阴离子所带电荷数= N(阴离子)×2=2NA,故B错误;n(Cl2)=22.4L÷22.4L/mol=1mol,Cl2与NaOH反应时既
本题难度:简单
4、选择题 在两个容积不同的容器中,一个盛有HCl气体,另一个盛有H2和C12(黄绿色气体)的混合气体。在同温同压下,两容器内的气体可能具有相同的[???? ]
A.分子数
B.颜色
C.原子数
D.密度
参考答案:D
本题解析:
本题难度:简单
5、选择题 NA代表阿伏加德罗常数值,下列说法正确的是
A.78gNa2O2所含有的离子数为3NA
B.1mol甲基中含有电子数为10NA
C.7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA
D.1molC10H22分子中共价键总数为22NA
参考答案:A
本题解析:A:Na2O2所含有的离子为Na+及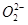 ,个数比2:1,故78gNa2O2(1mol)所含有的离子数为3NA,正确
,个数比2:1,故78gNa2O2(1mol)所含有的离子数为3NA,正确
B:甲基为中性原子团,含有9个电子,故1mol甲基中含有电子数为9NA
C:氯气与碱液发生的是自身氧化还原反应:Cl2+2NaOH=NaCl+NaClO+H2O
本题难度:简单