微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (4分)氧族元素位于周期表中?????????族,它们的最外层电子数为????????,该族元素随着核电荷数的递增,半径逐渐?????????,非金属性逐渐?????????。
2、选择题 在元素周期表中,分别与周期数、主族序数相同的一组是()
①质子数 ②核电荷数 ③电子层数 ④原子序数 ⑤最外层电子数
A.③⑤
B.②③
C.③④
D.①⑤
3、选择题 A、B分别为第三周期和第四周期的同一主族不同元素的原子,它们原子核内的质子数都等于中子数①若A为IIA族,其质量数为x,则B的质子数为y ②若A为ⅣA族,其质子数为m,则B的质量数为n,在下列各组值中,y和n的值分别是
A.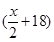 和
和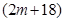
B.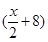 和
和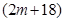
C.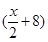 和
和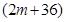
D.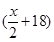 和
和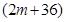
4、填空题 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数。R是由A、D两元素形成的离子化合物,其中A+与D2一离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体内晶体类型应属于???????(填写“六方”、“面心立方”或“体心立方”)堆积,空间利用率为?????????。
(2)C3-的电子排布式为????????????,在CB3分子中C元素原子的原子轨道发生的是???杂化,CB3分子的VSEPR模型为????????????。
(3)C的氢化物在水中的溶解度如何??????,为什么具有这样的溶解性??????????。
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是:?????????????
(用元素符号表示);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:??????????????????。
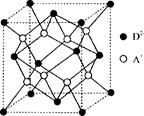
(5)如图所示是R形成的晶体的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是p g・cm-3试计算R晶体中A+和D2-最短的距离??????????????。
(阿伏加德罗常数用NA表示,只写出计算式,不用计算)
5、填空题 (16分)等电子原理的基本观点是:原子数相同且价电子总数相等的分子或离子具有相同的化学键类型和空间构型,互称为等电子体。等电子体的结构相似,物理性质相近。如:N2、CO与C22-、CN-为等电子体。
(1)已知CaC2为离子化合物,则CaC2的电子式为????????????????。
(2)聚丙烯腈俗称人造羊毛,由丙烯腈分子CH2=CH―CN经聚合反应生成;则CH2=CH―CN中C原子的杂化方式为?????????;分子中σ键和π键数之比为??????????。
(3)CO常与过渡金属原子M形成配合物M(CO)n ,其中满足中心原子价电子数与配位体提供电子总数之和为18,若M为Fe,则n=???????。
(4)CO与N2的结构相似,分子中含有共价三键,可表示为C≡O ;下表是两者的键能数据(单位:kJ・mol-1)
?
| C-O
| C=O
| C≡O
|
CO
| 357.7
| 798.9
| 1071.9
|
?
| N-N
| N=N
| N≡N
|
N2
| 154.8
| 418.4
| 941.7
CO与N2中化学性质较活泼的是???????;结合数据说明原因?????????????????????????????????。
(5)Fe3+,Fe2+,Co3+,Co2+都能与CN-形成配合物。硫酸亚铁溶液中加入过量KCN溶液,可析出黄色晶体K4[Fe(CN)6];若在上述溶液中再通入氯气后,可析出深红色晶体K3[Fe(CN)6];在K4[Fe(CN)6]和K3[Fe(CN)6]晶体中都不存在的微粒间作用力是??????????????????。(填标号)
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力
(6)写出与NO3-互为等电子体的分子????????????(写出一种)。
|