微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 正确的存放化学药品,是化学实验基本要求之一,下列物质存放错误的是
A.漂白粉长期敞口露置于空气中
B.金属钠保存在煤油中
C.NaOH溶液试剂瓶用橡胶塞
D.氯水在棕色试剂瓶中避光存放
参考答案:A
本题解析:略
本题难度:一般
2、实验题 (11分)实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:
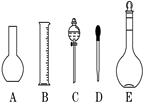
(1)如图所示的仪器中配制溶液肯定不需要的是 ?(填序号),
仪器C的名称是??????????,
本实验所需玻璃仪器E规格为 ?mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.量取一定体积的液体
(3)在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线, 则所配制溶液浓度
?????????0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
参考答案:(1)? AC(1分) 分液漏斗(1分)
(2) 5
本题解析:考查溶液的配制
(1)在配制过程中,不需要A:平底烧瓶、C:分液漏斗
根据容量瓶的规格可知,选用略大于450ml的,即500ml
(2)容量瓶唯一的作用就是配制溶液,没有其它作用,故BCD符合题意
(3)定容时仰视刻度线,会导致加水偏多,浓度偏小。
若NaOH溶液未冷却即转移至容量瓶,由于热膨胀,定容时加少量会偏少,最终溶液浓度偏高
(4)0.5×0.5=V×1.84×98%/98,求得V=13.6ml;很明显,应选用容积略大于13.6ml的25ml量筒
本题难度:简单
3、选择题 实验是化学研究的一种重要手段,现有下图所示A~G七种仪器,请根据要求填空。

(1)写出仪器名称:E???????????,F?????????????
(2)下列实验操作中用到仪器G的是???????????????(选填下列选项的编号字母)。
a.分离水和CC14的混合物?
b.分离水和酒精的混合物?
c.分离水和泥砂的混合物
(3)实验室配制100mL 0.5mol/L的盐酸溶液。
①下列关于仪器E的使用方法中,正确的是????????????(选填下列选项的编号字母)。
a.使用前应检查是否漏液????????????????????????? b.使用前必须烘干
c.不能用作物质反应或溶解的容器????????????? d.热溶液可直接转移到容量瓶中
②需要10mol/L的浓盐酸????????????mL。取用该体积盐酸时,需要用到上述仪器中的A和????????????(选填仪器的编号字母)。
参考答案:(1)容量瓶,冷凝管(2)a??(3)① ac ?② 5(或
本题解析:
试题分析:(1)根据仪器的结构特点判断仪器的名称;E为容量瓶,F为冷凝管;(2)G为分液漏斗,可用于分离互不相溶的液体混合物;选a;(3)①E为容量瓶,只能在常温下使用,且只能用来配制溶液,不能用作它途,且使用前要检查是否漏水,答案为:ac;②根据稀释定律计算所需浓盐酸的体积;0.1L×0.5mol/L=10moL/L×V,V=0.005L,即5 91EXAM.org.0mL,取用该体积盐酸时,需要用到上述仪器中的量筒和胶头滴管,其中胶头滴管用于定容,答案为:5.0;C。
本题难度:一般
4、选择题 在测定硫酸铜晶体结晶水含量实验中,下列操作会引起晶体中结晶水的质量分数偏大的是(??)
A.加热后在空气中冷却称量
B.粉末未完全变白就停止加热,进行称量计算
C.加热时间过长,部分变黑
D.两次称量结果相差0.2g就不再继续加热而进行计算
参考答案:C
本题解析:略
本题难度:简单
5、选择题 下列有关实验的说法正确的是
A.将氯化铝溶液加热蒸发、烘干可得无水氯化铝固体
B.测量溶液的导电性可区分出试剂盐酸和醋酸,导电能力强的是盐酸
C.做完银镜反应后的试管可用热的稀硝酸清洗,回收后的硝酸银溶液可再利用
D.除去硫酸铝溶液中混有的硫酸镁,可加入足量烧碱,过滤,向滤液中加入适量硫酸酸化
参考答案:C
本题解析:A因为氯化铝在水溶液中水解,且生成的HCl易挥发,故蒸干氯化铝溶液得到的是Al(OH)3固体而不是氯化铝固体;B因没有说明盐酸和醋酸物质的量浓度的大小关系,故溶液导电性不好比较。
本题难度:一般