微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 现对0.1mol/L的纯碱溶液进行相关研究.
(1)用pH试纸测定该溶液的pH,其正确的操作______.
(2)由上测得纯碱溶液呈碱性,请用离子方程式表示其原因:______.
(3)某同学根据所学知识对Na2CO3溶液进行分析,写出了以下四个关系式.请你判断:在正确的关系式后面打“√”,在错误的后面写出正确的关系式.
①c(Na+)=2[c(CO32-)+c(HCO3-)]:______;
②c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-):______;
③c(OH-)=c(H+)+c(HCO3-)+c(H2CO3):______;
④c(Na+)>c(CO32-)>c(OH-)>c(HCO3-):______.
2、选择题 把0.02 mol・L-1 CH3COOH溶液与0.01 mol・L-1 NaOH溶液等体积混合,则混合液中微粒浓度关系正确的是
[???? ]
A.c(CH3COO-)>c(Na+)
B.c(CH3COOH)>c(CH3COO-)
C.2c(H+)=c(CH3COO-)-c(CH3COOH)
D.c(CH3COOH)+c(CH3COO-)=0.01 mol・L-1
3、填空题 直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(1)用化学方程式表示S形成硫酸酸雨的反应方程式______,______.
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是______.
(3)吸收液吸收SO2的过程中,pH随n(SO32-),n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91
pH
8.2
7.2
6.2
①上表判断NaHSO3溶液显______性,用化学平衡原理解释:______.
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):______.
a、c(Na+)=2c(SO32-)+c(HSO3-)
b、c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-)
c、c(Na+)+c(H-)=c(SO32-)+c(HSO3-)+c(OH-)
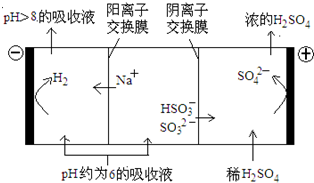
(4)当吸收液的pH降至约为6时,送至电解槽再生.再生示意图如图:
①HSO3-在阳极放电的电极反应式是______.
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用.简述再生原理:______.
4、填空题 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:

(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸____。
(2)不考虑其他组的实验结果,单从乙组情况分析,c是否一定等于0.2____(填“是”或“否”)。混合液中离子浓度c(A-)与c(Na+)的大小关系是________。
(3)由丙组实验结果分析,HA是____酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=____mol・L-1。 写出该混合溶液中下列算式的精确结果(不能做近似计算)。 c(Na+)-c(A-)=____mol・L-1??? c(OH-)-c(HA)=____mol・L-1
5、选择题 已知可发生反应:2Fe2+ +Br2 ==2Fe3+ +2Br-,2Fe3++2I- ==2Fe2+ +I2。向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。则下列有关说法中正确的是
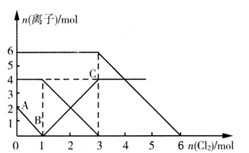 [???? ] [???? ]
A.还原性:Fe2+ >I-> Br-
B.当通入2 mol Cl2时,溶液中发生的离子反应可表示为2Fe2++2I-+2Cl2==2Fe3++I2+4Cl-
C.原混合溶液中FeBr2的物质的量为6 mol
D.原溶液中n(Fe2+):n(I-):n(Br-)=1:1:3
|