��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� NA��ʾ�����ӵ�������ֵ������������ȷ����????????????��???��
A��18g D2O�к��е�������Ϊ10NA
B��64gͭ����������ԭ��Ӧʧȥ�ĵ���������ΪNA
C����״���£�11.2L��ϩ�к��е�̼ԭ����Ϊ3NA
D��25��ʱ��1mol��L-1������Һ������CH3COOH��������һ��С��NA
�ο��𰸣�B
���������A��18g D2O�к��е�������Ϊ��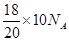 =9NA
=9NA
B�����統ͭ����Ӧʱ��������ͭ��64gͭ����������ԭ��Ӧʧȥ�ĵ�����ΪNA����ȷ
C����״���£���ϩ����̬������ȷ
D����Һ���δ����������������ȷ��������ȷ
��ΪB
�����Ѷȣ�һ��
2��ѡ���� ͬ��ͬѹ�£���������SO2��CO2��Ƚϣ�������������ȷ����[???? ]
A�������1��1
B�������16��11
C���ܶȱ�16��11
D���ܶȱ�11��16
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� �谢���ӵ�����ΪNA��������˵����ȷ����
A��100 g 98%��Ũ�����к���ԭ������Ϊ4NA
B�����³�ѹ�£�18g��ˮ(D2O)�������ĵ�����Ϊ10 NA
C�����³�ѹ�£�4.6 g NO2���庬��0.3 NA��ԭ��
D�������£�2.7g����ƬͶ��������Ũ�����У�������SO2��������Ϊ0.3NA
�ο��𰸣�C
������������⿼�鰢���ӵ�����.
100 g 98%��Ũ���������Ϊ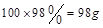 �������ʵ���Ϊ
�������ʵ���Ϊ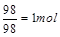 ��ÿ��
��ÿ�� �����Ѷȣ�һ��
�����Ѷȣ�һ��
4��ѡ���� ͬ��ͬѹ�£��ס����������ֱ�ʢ�м���Ͱ�������֪��������ԭ������ͬ����ס�����������������ǣ�???��
A��4�U3??????????? B��5�U4 ??????????? C��4�U5??????????????? D 1�U1
�ο��𰸣�C
���������
��ȷ�𰸣�C
����Ͱ��������ʵ�����Ϊ��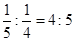
�����Ѷȣ���
5��ѡ���� �������ӵ���������ֵΪNA��������˵������ȷ����
A��1.0L0.1 mol��L��1Na2S��Һ�к��е�S2��������С��0.1NA
B��1 molFe�������������Ӧ��ת�Ƶ��ӵ���ĿΪ2 NA
C��2.24LCO��CO2��������к��е�̼ԭ����ĿΪ0.1NA
D��50mL18.4mol��L��1Ũ����������ͭ�ȷ�Ӧ������SO2���ӵ���ĿΪ0.46NA
�ο��𰸣�A
���������
���������n(Na2S)=0.1mol��L��1��1.0L=0.1mol��Na2S =2Na++ S2����n(S2��)= n(Na2S)=0.1mol������Na2S��ǿ�������Σ�S2����ˮ�⣬����Һ��n(S2��)<0.1mol����A��ȷ���������������ʿ�֪��2Fe+3Cl2=2FeCl3��6e��������ϵ��֮�ȵ������ʵ���֮�ȿ�֪��1mol�������������Ӧת��3mol���ӣ���B����ȱ�ٱ�״���£�����Ħ�������һ������22.4L/mol���������岻һ��Ϊ0.1mol������̼ԭ�Ӳ�һ��Ϊ0.1
�����Ѷȣ���