��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
����� �����ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr��OH��3������ȥ�����ֽ����������ɳ�����pH�����
| ��ʼ������pH | ��ȫ������pH
Fe��OH��2
7.0
9.0
Fe��OH��3
1.9
3.2
Cr��OH��3
6.0
8.0
��1��ij������ˮ��������Ҫ������ͼ��ʾ��
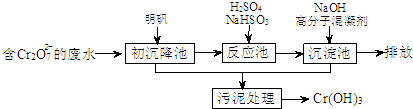
�ٳ������м����������������������õ�ԭ���ǣ������ӷ���ʽ��ʾ��______��
���벹�䲢��ƽ���·�Ӧ���з�����Ҫ��Ӧ�����ӷ���ʽ��
______Cr2O72-+______HSO3-+______�T______Cr3++______SO42-+______H2O��
�۸��ݡ����������͡��кͷ�����ԭ������������м���NaOH��Һ���˹����з�����Ҫ��Ӧ�����ӷ���ʽ�ǣ�H++OH-=H2O��______��֤��Cr3+������ȫ�ķ�����______��
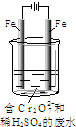
��2����ҵ���õ�ⷨ��������Cr2O72-��ˮ��ʵ����������ͼģ�����Cr2O72-�ķ�ˮ��������Ӧ��Fe-2e-=Fe2+��������Ӧʽ��2H++2e-=H2�� ��
��Fe2+��������Һ�е�Cr2O72-��Ӧ�����ӷ���ʽ��______��
��������Ӧ�õ��Ľ������������������ɳ�����ȫ�������ˮ�ĵ���ƽ��ǶȽ�����ԭ��______��
������Һ�к���0.01molCr2O72-����������ȫ�����ɳ��������ʵ�����______mol��
����� �����ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr��OH��3������ȥ�����ֽ����������ɳ�����pH�����
| ��ʼ������pH | ��ȫ������pH
Fe��OH��2
7.0
9.0
Fe��OH��3
1.9
3.2
Cr��OH��3
6.0
8.0
��1��ij������ˮ��������Ҫ������ͼ��ʾ��

�ٳ������м����������������������õ�ԭ���ǣ������ӷ���ʽ��ʾ��______��
���벹�䲢��ƽ���·�Ӧ���з�����Ҫ��Ӧ�����ӷ���ʽ��
______Cr2O72-+______HSO3-+______�T______Cr3++______SO42-+______H2O��
�۸��ݡ����������͡��кͷ�����ԭ������������м���NaOH��Һ���˹����з�����Ҫ��Ӧ�����ӷ���ʽ�ǣ�H++OH-=H2O��______��֤��Cr3+������ȫ�ķ�����______��
��2����ҵ���õ�ⷨ��������Cr2O72-��ˮ��ʵ����������ͼģ�����Cr2O72-�ķ�ˮ��������Ӧ��Fe-2e-=Fe2+��������Ӧʽ��2H++2e-=H2����
��Fe2+��������Һ�е�Cr2O72-��Ӧ�����ӷ���ʽ��______��
��������Ӧ�õ��Ľ������������������ɳ�����ȫ�������ˮ�ĵ���ƽ��ǶȽ�����ԭ��______��
������Һ�к���0.01molCr2O72-����������ȫ�����ɳ��������ʵ�����______mol ��

����𰸣���1����K2SO4�qAl2��SO4��3�q24H2OΪǿ�����
���������
�����������㣺�����ʵķ��롢�ᴿ��
�������׳̶ȣ���һ�㡿
No living man all things can. ����û�����ܵ���. |
|