微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT2+与ET2互为等电子体。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。
请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT2+的电子式_________;基态Z原子的核外电子排布式_________。
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有___________________________等两种。
(3)化合物甲由T、X两元素组成,其晶胞如图1,甲的化学式为_________。
(4)化合物乙的晶胞如图2,乙由E、Q两元素组成,硬度超过金刚石。
①乙的晶体类型为_________,其硬度超过金刚石的原因是___________________________。
②乙的晶体中E、Q两种元素原子的杂化方式均为__________________。

参考答案:(1) ;1s22s22p63s23p63d84s2
;1s22s22p63s23p63d84s2
(2)这两种氢化物均为极性分子、相互之间能形成氢键
(3)KO2?
(4)①原子晶体;C-N键的键长小于C-C键,键能大于C-C键;②sp3
本题解析:
本题难度:一般
2、选择题 关于氢键,下列说法正确的是
[? ]
A.每一个水分子内含有两个氢键
B.H2O、NH3、HF的熔沸点明显高于同主族其他非金属元素气态氢化物的熔沸点是由于它们的分子间有氢键的存在
C.H2O是一种非常稳定的化合物,这是由于氢键所致
D.氨气极易溶于水,重要的原因之一是由于氨分子与水分子之间能形成氢键
参考答案:BD
本题解析:
本题难度:简单
3、填空题 化学键的键能是指气态原子间形成1mol化学键时释放的能量。如:H(g)+I(g)→H-I(g)+297KJ 即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297KJ的热量。化学反应的发生可以看成旧化学键的破坏和新化学键的形成。下表是一些键能数据。(单位:kJ/mol)
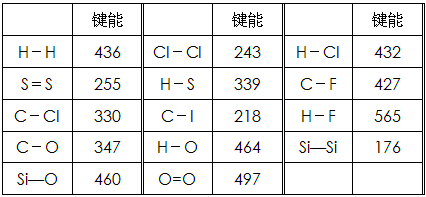
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性_________(填“大于”或“小于”)CF4的稳定性。试预测C-Br键的键能范围_________<C-Br键能<_________
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)=2HCl(g) ΔH=-QKJ/ mol;通过计算确定热化学方程式中Q的值为______________
(3)有人认为:H-O键的键能大于H-S键的键能,所以H2O的熔沸点高于H2S的熔沸点。你是否赞同这种观点?如不赞同,请说出你的解释。________________________________________
(4)①Si-Si键能小于Si-O键能的理由是:________________________________
②请写出晶体硅与氧气反应生成二氧化硅的热化学方程式:______________________________
参考答案:(1)小于;218KJ・mol-1;330KJ・mol-1
(2)185
(3)不赞同,H2O的熔沸点高于H2S是因为水分子间存在氢键,与键能无关
(4)①Si原子半径大于O原子,所以Si-Si的键长大于Si-O的键长,因而前者键能小于后者
②Si(s)+O2(g)=SiO2(s) △H=-991kJ/mo1
本题解析:
本题难度:一般
4、选择题 下列事实,不能用氢键知识解释的是
[? ]
A.水和乙醇可以完全互溶
B.氨气容易液化
C.干冰易升华
D.液态氟化氢化学式有时写成(HF)n的形式
参考答案:C
本 91exam.org题解析:
本题难度:一般
5、选择题 范德华力为akJ/mol,化学键为bkJ/mol,氢键为ckJ/mol,则a、b、c的大小关系是
[? ]
A.a>b>c
B.b>a>c
C.c>b>a
D.b>c>a
参考答案:D
本题解析:
本题难度:简单