微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55~60℃反应。已知苯与硝基苯的基本物理性质如下表所示:

某同学设计如图:
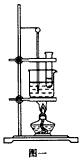
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是____________________________________
(2)分离硝基苯和水的混合物的方法是_____________;分离硝基苯和苯的方法是______________。
(3)某同学用图一装置制取硝基苯:
①用水浴加热的优点是_____________________;
②指出该装置的两处缺陷_____________________;_________________。
参考答案:(1)把浓硫酸缓慢加入浓硝酸中并不断搅拌
(2)分液;蒸馏
(3)可以使反应物受热均匀,并且温度容易控制;盛放反应物的试管部分应置于水面以下应在试管口加一个长直玻璃管起冷凝回流作用
本题解析:
本题难度:一般
2、实验题 某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
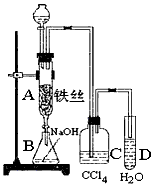
(1)写出A中反应的化学方程式:__________________________
(2)观察到A中的现象是:__________________________
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_____________________,写出有关的化学方程式__________________________
(4)C中盛放CCl4的作用是__________________________
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_________________,现象是__________________________。
参考答案:(1)C6H6+Br2 C6H5Br+HBr↑
C6H5Br+HBr↑
(2)反应液微沸,有红棕色气体充满A容器
(3)除去溶于溴苯中的溴;Br2+2NaOH==NaBr+NaBrO+H2O(或2Br2+6NaOH==5NaBr+NaBrO3+3H2O) (4)除去溴化氢气体中的溴蒸气
(5)石蕊试液;溶液变红色
本题解析:
本题难度:一般
3、填空题 工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾(?FeSO4?7H2O?).
(1)若用98%?1.84g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1:______.
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00g铁粉充分反应,收集到224mL(标准状况)气体,剩余固体质量为3.88g,测得反应后的溶液中Fe2+的物质的量为0.14mol(不含Fe3+).则该样品中Fe2+离子的氧化率为______.
(3)硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液.现取0.4g?Cu2S和CuS的混合物在酸性溶液中用40mL?0.150mol/L?KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O,6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O,反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与V?mL?0.2mol/L?(NH4)2Fe(SO4)2溶液完全反应.已知:MnO4-+Fe2++H+--Mn2++Fe3++H2O(未配平)①V的取值范围为______;②若V=35,试计算混合物中CuS的质量分数.
参考答案:(1)设浓硫酸的体积为xmL,水的体积为ymL;稀释前后硫酸的质量不变,
所以1.84x×98%1.84x+1.0y×100%=28%,解得x:y=1:4.6,故答案为:4.6;
(2)设与酸反应生成氢气需要的铁的质量为x,生成的硫酸亚铁的物质的量为y,
? Fe+2H+=Fe 2++H2 ↑
? ?56g?1mol?22.4L
? x?y?0.224L
解得x=0.56g,y=0.01mol,
与Fe3+反应需要的铁的质量为5.00g-3.88g-0.56g=0.56g,
与铁反应需要的三价铁离子的物质的量为m,生成的二价铁离子的物质的量为n,
Fe+2Fe3+=3Fe2+
56g?2mol?3mol
0.56g m?n
解得m=0.02mol,n=0.03mol,
所以原来溶液中二价铁离子的物质的量为0.14mol-0.01mol-0.03mol=0.1mol,
所以氧化率为0.02mol0.1mol+0.02mol=16.7%,
?故答案为:16.7%;
(3)①高锰酸钾的物质的量为:0.040L×0.150mol/L=0.006mol,
假设固体混合物全部为Cu2S,需要高锰酸钾的物质的量为x,
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
8? 5
x? 0.4g160g
x=0.004mol
剩余的高锰酸钾的物质的量为0.006mol-0.004mol=0.002mol,
0.002mol高锰酸钾和(NH4)2Fe(SO4)2溶液完全反应.
?MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
1mol?5mol
0.002mol?1×10-3VL×0.2mol/L
解得V=50,
假设固体混合物全部为CuS,需要高锰酸钾的物质的量为y,
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
6? 5
y?0.4g96g
y=0.005mol
剩余的高锰酸钾的物质的量为0.006mol-0.005mol=0.001mol.
0.001mol高锰酸钾和(NH4)2Fe(SO4)2溶液完全反应.
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
1mol? 5mol
0.001mol? 1×10-3VL×0.2mol/L
解得V=25,
故答案为:25<V<50;?
?②若V=35,与35mL(NH4)2Fe(SO4)2溶液完全反应需要高锰酸钾的物质的量为:
? MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
? 1mol? 5mol
0.014mol?0.035L×0.2mol/L
所以高锰酸钾的物质的量为0.0014mol,
故与固体混合物反应的高锰酸钾的物质的量为0.006mol-0.0014mol=0.0046mol,
设Cu2S的质量为xg,CuS的质量为yg,x+y=0.40g.
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
8mol? 800g
0.01xmol?xg
?6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
?6mol?480g
0.0125ymol?yg
本题解析:
本题难度:一般
4、实验题 实验室制备乙酸乙酯,回答有关问题:
(1)乙醇、乙酸和浓硫酸混合时,应怎样操作?为什么? _______________。
(2)收集乙酸乙酯的试管内盛有的饱和碳酸钠溶液的作用是 什么? ______________。
(3)反应中浓硫酸的作用是什么? _______________。
(4)反应中乙醇和乙酸的转化率能达到百分之百吗? _________________。
(5)收集在试管内的乙酸乙酯是浮在碳酸钠溶液上层,还是 沉在试管底部,还是与NaCO3溶为一体?为什么? _________________。
(6)用什么方法将收集到的乙酸乙酯分离出来? _____________。
参考答案:(1)乙醇与浓硫酸混合时放热,且浓硫酸的密度大于乙醇,所以混合时应向乙醇中慢慢加入浓硫酸和乙酸
(2)吸收蒸出的乙醇和乙酸,降低乙酸乙酯在水层中的溶解度,便于分层析出
(3)浓硫酸是催化剂和吸水剂
(4)不能。因为是可逆反应
(5)浮在上层,因乙酸乙酯不溶于水且比水轻
(6)用分液漏斗分液
本题解析:
本题难度:一般
5、选择题 下列关于实验的叙述正确的是
[? ]
A.向煮沸的1 mol/L NaOH溶液中滴加饱和FeCl3溶液制备Fe(OH)3胶体
B.直接观察焰色反应,火焰为浅紫色,则一定不含Na元素
C.若酸碱用量不同,则相同条件下测得的中和热数值也不同
D.将二氧化锰和0.5 mol/L盐酸混合加热,制取氯气
参考答案:B
本题解析:
本题难度:一般