��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣���֪A��JΪ�����������ʣ�������BΪҺ�廯���E�ǿ�������Ҫ�ɷ�֮һ��L����ɫ������HΪ����ɫ���壻����֮���ת����ϵ����ͼ��ʾ��?
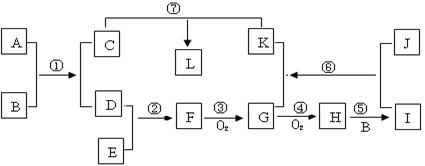
��1��H�Ļ�ѧʽ��________��
��2���۵Ļ�ѧ����ʽ��__________________________________��
��3�������ӷ���ʽ��_______________________________��
��4��F������________�����������ķ�����___________________________________��
�ο��𰸣���10�֣�
��1��H�Ļ�ѧʽ��___ NO2___��?
��2���۵Ļ�ѧ����ʽ��____________ NH3_+__ O2 NO+H2O_______��?
NO+H2O_______��?
��3�������ӷ� ��ʽ��____3Cu__+8HNO3__
��ʽ��____3Cu__+8HNO3__ 2NO�� +3Cu(NO3) 2__+__ 4H2O ______��
2NO�� +3Cu(NO3) 2__+__ 4H2O ______��
��4��_������_�ò�����պȡŨ�����쵽װ�д�������Թܿڣ����а��������������Ϊ����_��
�����������
�����Ѷȣ�һ��
2������� �����ֳ���������ɵĻ����A���ں��ʵ������¿ɰ���ͼ���з�Ӧ�����ֲ����ˮʡ�ԣ�����֪FΪ���ɫ��������ش�

��1�������A�ijɷ��� ?�����ѧʽ����
��2��д����Ӧ�ٵ����ӷ���ʽΪ��??��
��3��д����Ӧ�ڵĻ�ѧ����ʽΪ��??��
�ο��𰸣���1��Fe? Al
��2��2Al+2OH-+2H2O= 2AlO2-+3H2��
 ?��3��4Fe(OH)2+O2+2H2O=4Fe(OH)3
?��3��4Fe(OH)2+O2+2H2O=4Fe(OH)3
�����������
�����Ѷȣ���
3������� ��6�֣���֪X�ǵ���ɫ���壬A��B���Σ�����ɫ��Ӧ�ʻ�ɫ��C�������Σ�D��E����ɫ���塣A��B��C��D��X֮���ת����ϵ ���£�
���£�
��1��A��H2SO4��ϡ����C��D������������2��B��H2SO4��C��E����H2O��
��3��D��E��X��H2O��������4��B��O2��C������5��X��NaOH��A��B��H2O
���ƶϻ�ѧʽ��A�ߣߣߣߣߣߣߣߣ�B�ߣߣߣߣߣߣߣ�C�ߣߣߣߣߣߣߣߣ�
D�ߣߣߣߣߣߣߣߣ�E�ߣߣߣߣߣߣߣ�X�ߣߣߣߣߣߣߣߡ�
�ο��𰸣�Na2S��Na2SO3��Na2SO4��H2S��SO2��S
�����������
�����Ѷȣ�һ��
4������� ����ͬѧ��̽��һ���غ�ɫ��״�������Ҫ�ɷ֣���������Ԫ����ɣ������ù�������ϡ�����������A�ų������õ�dz��ɫ��ҺB��A�ڿ����г��ȼ�գ��ֵõ���ɫ�д̼�����ζ������C����������ʹƷ����Һ��ɫ����B��Һ�м������������������Һ�����ȵõ���ɫ������Ȼ�����Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ��
��������ʵ������ش�
��1�����غ�ɫ��״�������Ҫ�ɷ��ǣ�д��ѧʽ��______��
��2��������д������������C���ɵ�������ԭ��Ӧ����ʽ��
��______��
��______��
��3����д����ɫ������ɺ��ɫ�����Ļ�ѧ����ʽ��______��
��4�������ɫ��������ϡ�������������Һ�еĽ��������ӣ���ѡ�õ��Լ���______��
�ο��𰸣����ù�������ϡ�����������A�ų������õ�dz��ɫ��ҺB��˵��B�к����Ȼ�������A�ڿ����г��ȼ�գ��ֵõ���ɫ�д̼�����ζ������C����������ʹƷ����Һ��ɫ����C�Ƕ�������A�����⣬��B��Һ�м������������������Һ�����ȵõ���ɫ������Ȼ�����Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ����˵��B���������Ȼ��������غ�ɫ��������ᷴӦ�����Ȼ����������⣬����غ�ɫ������FeS��
��1��ͨ�����Ϸ���֪��A�Ļ�ѧʽ��FeS���ʴ�Ϊ��FeS��
��2������������ȼ�����ɶ�������ͭ��Ũ�����ڼ��������·�Ӧ���ɶ������������䷽��ʽ�ֱ�Ϊ��
S+O2?��ȼ?.?SO2��Cu+2H2SO4��Ũ��?��?.?CuSO4+SO2 ��+2H2O��
�ʴ�Ϊ��S+O2?��ȼ?.?SO2��Cu+2H2SO4��Ũ��?��?.?CuSO4+SO2 ��+2H2O��
��3��������������������������������������Ӧ����ʽΪ4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��4�������Ӻ����軯����Һ��Ӧ����������ʹ��Һ��Ѫ��ɫ���ʴ�Ϊ��KSCN��Һ��
���������
�����Ѷȣ�һ��
5������� ����X��Y��Z���ַǽ���Ԫ�أ�A��B��C���ֽ���Ԫ�أ������������
��1��X��Y��Z�ĵ����ڳ����¾�Ϊ����
��2��X�ĵ�����Z�ĵ�����ȼ�գ�����ʲ�ɫ������XZ��ˮ��Һ��ʹʯ����Һ��졣
��3����Ħ��X�ĵ��ʿ���һĦ��Y�ĵ��ʻ���������Ħ��X2?Y��X2Y������ΪҺ�塣
��4��Z�ĵ�������X2Y��������Һ����Ư���ԡ�
��5��A�ĵ��ʿ�����Z�ĵ�����ȼ�գ������غ�ɫ���壬�ù�������ˮ�ʻ�ɫ��Һ��
��6��B��Z�γɵĻ�����BZ3����ˮ����εμ�NaOH��Һ�����ɰ�ɫ�����������ܽ⡣
��7��C�ĵ�����Y���ʷ�Ӧ���ܵõ����ֲ������һ��Ϊ����ɫ����M��
������������⣺
��д���������ʵĻ�ѧʽ��XZ??��X2Y??��M?��
��Z�ĵ�������X2Y��������Һ����Ư�����õ������� ?���ѧʽ��
��A�ĵ�����Z�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽ��?
��BZ3�������NaOH��Һ��Ӧ�����ӷ���ʽ��??��
��X������Z���ʵĻ�����徭��ȼ��ַ�Ӧ����ȴ�����£���ͨ��������NaOH��Һ�У����屻��ȫ���գ���ԭ���������X������Z���ʵ�����ȿ���Ϊ?��
�ο��𰸣���HCl? (1��)? H2O? (1��)? Na2O2?(1��) ?��HClO? (2��)
��2Fe+3Cl2?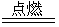 2FeCl3?(2��)
2FeCl3?(2��)
��Al3++4OH-?=AlO2-?+? 2H2O? (2��)
V(X)?��? V(Z)?�Q? 1?(3��)
���������X�ĵ�����Z�ĵ�����ȼ�գ�����XZ��ȼ��ʱ����ʲ�ɫ��XZ������ˮ��XZ��ˮ��Һ��ʹʯ����Һ��죬˵��XΪHԪ�أ�ZΪClԪ�أ��γɵĻ�����ΪHCl����Ħ��X�ĵ��ʿ���һĦ��Y�ĵ��ʻ���������Ħ��X2Y��X2Y������ΪҺ�壬ӦΪH2O����YΪOԪ�ء�A�ĵ��ʿ�����Z�ĵ�����ȼ�գ������غ�ɫ���壬�ù�������ˮ���ػ�ɫ��Һ�����غ�ɫ����ΪFeCl3����AΪFeԪ�ء�B��Z�γɵĻ�����BZ3����ˮ����εμ�NaOH��Һ�����ɰ�ɫ�����������ܽ⡣��BZ3ΪAlCl3��BΪAl��C�ĵ�����Y���ʷ�Ӧ���ܵõ����ֲ������һ��Ϊ����ɫ���õ���ɫ����ΪNa2O2����CΪNa���������Ϸ�����֪��XZΪHCl��X2YΪH2O��BZ2ΪCuCl2������ɫ����MΪNa2O2����Cl�ĵ�������H2O�з�Ӧ����HCl��HClO������HClO����Ư���ԡ���Fe��Cl2��ȼ�����ɣ���Ӧ�Ļ�ѧ����ʽΪ2Fe+3Cl2 2FeCl3����BZ3�������NaOH��Һ��Ӧ�����ӷ���ʽ��Al3+?+? 4OH-?=? AlO2-?+? 2H2O�������ڹ������������ܷ�����Ӧ2NaOH+Cl2=NaCl+NaClO+H2O�����������ܷ����˷�Ӧ��Ҫ��֤������ȫ������ֻҪȷ�������������������С�ڵ���1���С�
2FeCl3����BZ3�������NaOH��Һ��Ӧ�����ӷ���ʽ��Al3+?+? 4OH-?=? AlO2-?+? 2H2O�������ڹ������������ܷ�����Ӧ2NaOH+Cl2=NaCl+NaClO+H2O�����������ܷ����˷�Ӧ��Ҫ��֤������ȫ������ֻҪȷ�������������������С�ڵ���1���С�
�����Ѷȣ�һ��