微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在指定的条件下,下列各组离子一定能大量共存的是( )
A.无色的溶液中:Fe3+、K+、NO3-、Cl-
B.pH=13的溶液中:NH4+、Na+、SO42-、Cl-
C.含有大量Ba2+的溶液中:NH4+、Na+、Cl-、H+
D.c(H+)=0.1?mol?L-1的溶液中:K+、I-、Cl-、NO3-
参考答案:A.因Fe3+为黄色,与无色溶液不符,故A不选;
B.pH=13的溶液,显碱性,NH4+、OH-结合生成弱电解质,则不能共存,故B不选;
C.该组离子之间不反应,则能够共存,故C选;
D.因H+、I-、NO3-发生氧化还原反应,则不能 共存,故D不选;
故选C.
本题解析:
本题难度:一般
2、填空题 (12分)有一固体混合物,可能由NaI、KCl、Na2CO3、Na2SO4、CaCl2、Cu(NO3)2中的一种或几种组成,为了检验所含的物质,做了以下实验:
①取少许固体溶于水,得到无色透明溶液;②往此溶液中滴加氯化钡溶液,有白色沉淀生成;③过滤,往沉淀中加入足量的稀硝酸,发现沉淀没有全部溶解且有无色无味的气体生成。④往滤液中加入足量的新制的氯水,再加入少许汽油,振荡,静置,上层液体呈紫红色。
(1)试判断:固体混合物中肯定含有 ,一定没有 ,可能含有________________。
(2)对可能含有的物质,如何进行实验以进一步检验。
(3)实验④中发生的化学反应属于 反应(填反应类型),主要实验操作名称叫
参考答案:(1)肯定含有Na2CO3、Na2SO4、NaI,一定没有Cu(NO3)2、CaCl2,可能含有KCl
(2)做焰色反应,若透过蓝色钴玻璃有紫色火焰,则含KCl;反之,则没有。
(3)置换反应或氧化还原反应 萃取
本题解析:(1)由①,无Cu(NO3)2,且CaCl2和Na2CO3不能同时有;由②,有Na2CO3,无CaCl2;由③,“部分溶于”有Na2SO4;由④,上层紫红色,上层是苯(萃取,苯密度小于水,易溶解碘),有KI,因此不能确定KCl;因此有Na2SO4,Na2CO3、 KI;无CuCl2、CaCl2,可能有KCl(2)检验氯化钾,可以做焰色反应。若透过蓝色钴玻璃有紫色火焰,则含KCl;反之,则没有。(3)实验④中发生的化学反应Cl2+2I-=I2+2Cl-,发生的是氧化还原反应。加入有机溶剂萃取碘单质。
考点:利用物质的性质对物质进行检验。
本题难度:一般
3、填空题 离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在________(填编号)。
①单质?②氧化物?③电解质?④盐?⑤化合物
(2)一种无色透明溶液中,可能含有下列离子: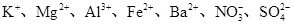 、
、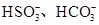 、I-和Cl-,取该溶液进行如下实验:
、I-和Cl-,取该溶液进行如下实验:
①将溶液滴在蓝色石蕊试纸上,呈红色。
②将少许溶液浓缩后加入铜片和硫酸,有无色气体析出,此气体通空气则立即变成红棕色。
③取少许溶液滴入BaCl2溶液,则产生白色沉淀。
④取实验③中的澄清溶液,滴入AgNO3试液,产生不溶于稀硝酸的白色沉淀。
⑤另取少许溶液,滴入NaOH溶液,有白色沉淀生成,当NaOH过量时,又有部分白色沉淀溶解。
根据以上现象判断,原溶液中肯定不存在的离子是_______;肯定存在的离子是_______;不能作出判断的离子是_______。
参考答案:(1)③⑤? (2)Fe2+、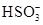 、
、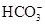 、I-、Ba2+
、I-、Ba2+
Mg2+、Al3+、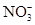 、
、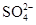 ? K+、Cl-
? K+、Cl-
本题解析:(1)有离子参与或生成的反应是离子反应,只要有离子,就必有电解质,而电解质属于化合物。
(2)由无色溶液知,溶液中一定不存在Fe2+;由实验①知,溶液呈酸性,则Mg2+、Al3+、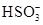 中至少存在一种;由实验②知,溶液中一定存在
中至少存在一种;由实验②知,溶液中一定存在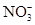 ;由实验③知,溶液中一定存在
;由实验③知,溶液中一定存在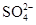 ,则溶液中一定不存在Ba2+;由于实验③中已经引入Cl-,所以由实验④无法确定Cl-的存在;由实验⑤知,产生的白色沉淀部分溶解,则溶液中一定存在Mg2+和Al3+,则溶液中一定不存在
,则溶液中一定不存在Ba2+;由于实验③中已经引入Cl-,所以由实验④无法确定Cl-的存在;由实验⑤知,产生的白色沉淀部分溶解,则溶液中一定存在Mg2+和Al3+,则溶液中一定不存在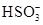 和
和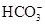 ?(水解相互促进反应);由于溶液呈酸性,且存在
?(水解相互促进反应);由于溶液呈酸性,且存在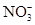 ,所以溶液中一定不存在I-。综合分析:溶液中肯定不存在的离子是:Fe2+、
,所以溶液中一定不存在I-。综合分析:溶液中肯定不存在的离子是:Fe2+、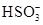 、
、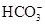 、I-、Ba2+,溶液中肯定存在的离子是:Mg2+、Al3+、
、I-、Ba2+,溶液中肯定存在的离子是:Mg2+、Al3+、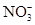 、
、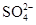 ,溶液中无法确定的离子是:K+、Cl-
,溶液中无法确定的离子是:K+、Cl-
本题难度:一般
4、选择题 下列粒子在溶液中能大量共存的一组是(? )
A.H+、Fe2+、SO42-、C12
B.K+、Ag+、NH3・H2O、NO3-
C.Mg2+、Na+、SO42-、Cl- .
D.Na+、A13+、Cl-、HCO3-
参考答案:C
本题解析:A、溶液中Fe2+和C12发生反应:Cl2 + 2Fe2+====2Fe3+ + 2Cl-,不能大量共存,错误;B、溶液中Ag+和NH3・H2O发生反应,生成氢氧化银沉淀或银氨络离子,不能大量共存,错误;C、题给条件下,组内离子间不反应,能大量共存,正确;D、溶液中A13+和HCO3-水解相互促进生成氢氧化铝沉淀和二氧化碳气体,不能大量共存,错误。
本题难度:一般
5、选择题 下列各组离子一定能大量共存的是
A.在含大量Ag+的溶液中:NH4+、Na+、I-、NO3-
B.在酚酞呈红色的溶液中:Na+、K+、AlO2-、CO32-
C.由水电离出的c(H+)=10-13mol・L-1的溶液中:NH4+、HCO3-、SO42-、NO3-
D.无色溶液中:K+、Cu2+、Na+、SO42-
参考答案:B
本题解析:A中Ag+和I-生成AgI,I-不能大量共存,A错误;酚酞呈红色的溶液是碱性溶液,B中离子可以大量共存,B正确;常温下,水电离出的c(H+)=10-13mol/L的溶液pH=1或13,HCO3-两种情况下都不能大量共存,NH4+在强碱溶液中也不能大量共存,C错误;D中Cu2+呈蓝色,D错误。
点评:离子不能大量共存一般有如下几种情况:生成沉淀、气体、水、弱电解质、发生氧化还原反应等,此外要注意题中限制条件。
本题难度:一般