微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于钠原子和钠离子,下列叙述中错误的是
[? ]
A.它们相差一个电子层
B.它们的化学性质相似
C.钠原子半径比钠离子半径大
D.钠离子和钠原子均为同一元素
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列说法正确的是( )
A.在元素周期表中,元素所在族的族序数等于原子核外最外层电子数
B.在元素周期表中,元素所在的周期数等于原子核外电子数
C.最外层电子数为8的微粒是稀有气体元素的原子
D.同主族元素的原子序数越大,其原子半径越大
参考答案:A、主族元素的族序数等于最外层电子数,但副族元素不一定,如锰处于第ⅦB族,外围电子排布为3d54s1,故A错误;
B、元素所在的周期数等于电子层数(钯除外),故B错误;
C、最外层电子数为8的微粒,若是中性原子则是稀有气体元素的原子,若是离子则不是,如S2-等,故C错误;
D、同主族元素的原子序数越大,电子层越多,电子层的影响比核电荷数大,原子半径增大,故D正确.
故选D.
本题解析:
本题难度:一般
3、选择题 下列说法中,肯定错误的是
[? ]
A.某原子在K层上只有一个电子 ?
B.某原子M层上电子数为L层上电子数的4倍 ?
C.某离子M层上电子数为K层上电子数的4倍 ?
D.某离子的核电荷数与最外层电子数相等
参考答案:B
本题解析:
本题难度:简单
4、填空题 有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在B单质中燃烧时呈现黄色火焰,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)元素名称:A______?C______
(2)写出AB2?的电子式为______
(3)画出D的原子结构示意图______,用电子式表示化合物?C2D?的形成过程______.
参考答案:A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,A的L层电子数是K层电子数的两倍,则A有2个电子层,L层电子数为4,故A为碳元素;D单质颜色是淡黄色固态化合物,则D为硫元素;A和B原子有相同的电子层数,且C在B单质中燃烧时呈现黄色火焰,则B为氧元素,C为钠元素,生成化合物为过氧化钠.
(1)由上述分析可知,A为碳元素;C为钠元素.
故答案为:碳;钠.
(2)AB2?是CO2,分子中碳原子与氧原子之间形成2对共用电子对,电子式为
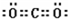
.
故答案为:
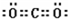
.
(3)D为硫元素,原子核外有16个电子,有3个电子层,最外层有6个电子,的原子结构示意图为
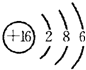
.?C2D?为Na2S,由钠离子与硫离子构成,电子式表示Na2S的形成过程为

.
故答案为:

;

.
本题解析:
本题难度:简单
5、选择题 W粒子的结构示意图如图所示,下列关于它的说法不正确的是( )
A.Y=2
B.若X=18,则Z=8
C.若X=11,它的氧化物化学式为W2O
D.若X=15,它属于金属元素的原子
