微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某不纯的烧碱样品,含Na2CO3?3.8%(质量百分含量)、H2O?5.8%、NaHCO3?0.004%.取m?g样品溶于40mL?2mol?L-1的盐酸后,并用?2mol?L-1?NaOH溶液中和剩余的酸,在蒸发后可得干燥的固体的质量为
A.4.68g
B.5.58g
C.2.34g
D.无法计算
参考答案:A
本题解析:分析:样品加盐酸反应后剩余固体为NaCl,根据盐酸的物质的量可知NaCl的物质的量,进而计算质量.
解答:样品中Na2CO3、NaHCO3以及NaOH和盐酸反应最终产物都为NaCl,盐酸的物质的量为0.04L×2mol/L=0.08mol,
根据Cl元素守恒可知,生成固体NaCl的物质的量也为0.08mol,
则NaCl的质量为0.08mol×58.5g/mol=4.68g.
故选A.
点评:本题考查混合物的计算,题目难度不大,本题解题关键是判断最终产物的成分.
本题难度:简单
2、选择题 下列分离物质的方法中,根据粒子大小进行分离的是
A.萃取
B.重结晶
C.沉淀
D.渗析
参考答案:D
本题解析:所谓渗析就是利用半透膜能透过小分子和离子但不能透过胶体粒子的性质从溶胶中除掉作为杂质的小分子或离子的过程,故答案为D;注:萃取是根据物质在不同溶剂中的溶解度的差异进行分离的方法;重结晶是指将晶体溶于溶剂或熔融以后,又重新从溶液或熔体中结晶的过程。
本题难度:一般
3、选择题 除去SO2中混有的SO3气体,不能选用的试剂是
A.98.3% H2SO4
B.BaCl2溶液
C.饱和NaHSO3溶液
D.饱和NaHCO3溶液
参考答案:D
本题解析:分析:根据除杂原则,选择除杂剂最少要满足两个条件:①加入的试剂只能与杂质反应,或吸收杂质,不能吸收被提纯物质,不能与被提纯物质反应;②反应时不能引入新的杂质.注意生成被提纯的物质最好,结合选项中各物质的性质判断.
解答:A、98.3% H2SO4可以吸收SO3气体,不影响SO2气体,故A正确;
B、BaCl2溶液与SO2气体不反应,与SO3气体反应生成硫酸钡沉淀,除去SO3气体,故B正确;
C、饱和NaHSO3溶液与SO3、水反应,除去SO3气体,同时生成SO2气体,故C正确;
D、亚硫酸是中强酸,比碳酸酸性强,饱和NaHCO3溶液与SO2、水反应,SO2气体被吸收,故D错误.
故选:D.
点评:本题考查了二氧化硫和三氧化硫的性质应用,主要考查气体除杂的原则不增不减,简单易分离复原,最好.
本题难度:简单
4、选择题 溶液、胶体、浊液三种分散系最本质的区别是
A.稳定性
B.透明度
C.分散质微粒大小
D.能否发生丁达尔现象
参考答案:C
本题解析:分析:溶液、胶体、浊液三种分散系的分散剂都是液体,分散质都是固体,最本质的区别是分散质粒子的直径大小.
解答:当分散剂是水或其它溶液时,根据分散质微粒直径大小来分类,把分散系划分为:溶液(小于1nm)、胶体(1nm~100nm)、浊液(大于100nm),
所以,溶液、胶体和浊液这三种分散系的本质的区别在于分散质微粒直径大小.
故选C.
点评:注意:1、三类分散系的本质差异是分散质粒子的大小.2、利用分散系的组成不同,可以选择不同的方法进行分离提纯.
本题难度:简单
5、选择题 下列各物质中,不是按 (“→”表示一步完成)关系相互转化的是
(“→”表示一步完成)关系相互转化的是
A.A
B.B
C.C
D.D
参考答案:C
本题解析:分析:根据物质的性质判断反应能否发生,C中SiO2不能与水反应生成H2SiO3.
解答:A.可发生:Fe FeCl3
FeCl3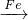 FeCl2
FeCl2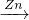 Fe,故A不选;
Fe,故A不选;
B.可发生:Cl2 NaClO
NaClO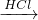 NaCl
NaCl Cl2,故B不选;
Cl2,故B不选;
C.SiO2不能与水反应生成H2SiO3,SiO2应先和碱反应生成Na2SiO3,然后再和酸反应生成H2SiO3,故C选;
D.可发生:HNO3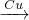 NO
NO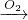 NO2
NO2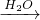 HNO3,故D不选.
HNO3,故D不选.
故选C.
点评:本题考查元素化合物知识,题目难度不大,本题注意把握常见元素化合物的性质.
本题难度:困难