��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��0.15 mol��MnO2�������12 mol��L��1��Ũ���ᷴӦ����50 mL 12 mol��L��1��Ũ������������MnO2��Ӧ���߲�����Cl2���(������Ӧ������ͬ)?
A��һ����?
B��ǰ�߽Ϻ��߶�?
C�����߽�ǰ�߶�?
D�����Ƚ�?
�ο��𰸣�B?
���������Ũ������������MnO2��Ӧʱ�����ŷ�Ӧ�Ľ��У�����Ũ�ȱ�С�����߷�Ӧ��ֹͣ����һ����HCl����ת���Cl2��
�����Ѷȣ�һ��
2��ѡ���� XԪ������������Ӧ��ˮ����ΪH3XO4��������Ӧ���� ̬�⻯��Ϊ
̬�⻯��Ϊ
A��HX
B��H2X
C��XH4
D��XH3
�ο��𰸣�D
�����������
�����Ѷȣ���
3������� ����ͼ��ʾװ�ÿ������һϵ��ʵ�飨ͼ�мг�װ������ȥ��
��ش��������⣺
��������a��Cl2��װ��A��B��C�е��Լ�����Ϊ��FeCl2��Һ������KI��Һ��ʯ����Һ��
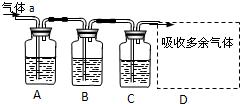
| װ�� | A | B | C | D
�Լ�
FeCl2��Һ
����KI��Һ
ʯ����Һ
______
����
��Һ��dz��ɫ��Ϊ�ػ�ɫ
______
______
���ӷ���ʽ
______
______
______
|
II������a��SO2��װ��A��B��C�е��Լ�����Ϊ��Ʒ����Һ�����Ը��������Һ�������ᣨ�����ˮ��Һ����
| װ�� | A | B | C
�Լ�
Ʒ����Һ
���Ը��������Һ
�����ˮ��Һ
����
______
��ɫ��ȥ
______
����SO2������
______
______
������
|
��1��д��C�з�����Ӧ�Ļ�ѧ����ʽ______��
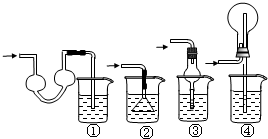
��2��Dװ����������������Һ������SO2��Ϊ�˷�ֹ������Ӧ��ѡ������װ���е�______������ţ���
�ο��𰸣���������a��Cl2��װ��A��B��C�е��Լ�����Ϊ��FeCl2��Һ������KI��Һ��ʯ����Һ��
������A���Ȼ�������Ӧ�����Ȼ������۲쵽��Һ��dz��ɫ��Ϊ��ɫ�����������ӷ�ӦΪCl2+2Fe2+=2Fe3++2Cl-��
��B�е���KI��Ӧ���ɵⵥ�ʣ��۲쵽��Һ���������������ӷ�ӦΪCl2+2I-=I2+2Cl-��
��C����ɫʯ����Һ�ȱ�����ɫ��DΪβ������װ�ã���D��NaOH��Ӧ����NaCl��NaClO��ˮ�����ӷ�ӦΪCl2+2OH-=Cl-+ClO-+2H2O���ʴ�Ϊ��װ��ABCD�Լ�NaOH��Һ������Һ�����ȱ�����ɫ���ӷ���ʽCl2+2Fe2+=2Fe3++2Cl-Cl2+2I-=I2+2Cl-Cl2+2OH-=Cl-+ClO-+2H2OII������a��SO2��װ��A��B��C�е��Լ�����Ϊ��Ʒ����Һ�����Ը��������Һ�������ᣨ�����ˮ��Һ����
��������ʹA��Ʒ����ɫ�����ֶ����������Ư���ԣ���B�и�����ط���������ԭ��Ӧ�������仹ԭ�ԣ���C�������ˮ��Һ����������ԭ��Ӧ�������ˮ���۲쵽��������ɫ�����������������ԣ��ʴ�Ϊ��
װ��ABC�Լ������ɫ��ȥ���ɵ���ɫ��������SO2������Ư���Ի�ԭ�ԣ�1��C�ж������������ⷴӦ�������ˮ���÷�ӦΪSO2+2H2S�T3S��+2H2O���ʴ�Ϊ��SO2+2H2S�T3S��+2H2O��
��2��������װ�ò����������ѹǿ����ܷ�ֹ������ͼ�Т٢۾��л�������νṹ�������γ�ѹǿ�����������������ã��ʴ�Ϊ���٢ۣ�
���������
�����Ѷȣ�һ��
4������� ��1�����Ʊ�����ˮ�д�������������ˮ�ʻ���ɫ��˵����ˮ�к���______�������ʽ����������Na2CO3���д�����ɫ���������˵����ˮ�к���______�������ӷ��ţ���������AgNO3��Һ�����а�ɫ����������˵����ˮ�к���______�������ӷ��ţ�����������ɫīˮ��īˮ����ɫ��˵����ˮ�к���______�������ʽ��
��2�����������������
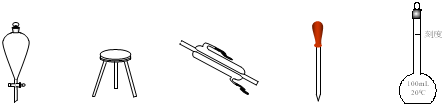
��______?��______?��______?��______?��______��
�ο��𰸣���1����������ˮ��ˮ�����ܽ������������ʻ���ɫ��������ˮ��Ӧ��Cl2+H2O=H++Cl-+HClO����Һ�����ԣ�����Na2CO3���д�����ɫ�������������AgNO3��Һ�����а�ɫ����������HClO����ǿ�����Ժ�Ư���ԣ�������ɫīˮ��īˮ����ɫ��
�ʴ�Ϊ��Cl2��H+��Cl-��HClO��
��2����Ϊ��Һ©������Ϊ���Ǽܣ���Ϊ�����ܣ���Ϊ��ͷ�ιܣ���Ϊ����ƿ��
�ʴ�Ϊ����Һ©�������Ǽܣ������ܣ���ͷ�ιܣ�����ƿ��
���������
�����Ѷȣ�һ��
5��ѡ���� ����������������ˮ������������������Һ����NaOH ��AgNO3 ��Na2CO3 ��FeSO4 ��KI ��Na2S
��Na2SO3 ��ʹ���Ƶ���Һ���ʵ���
[? ]
A���ܢ�
B���ڢܢݢ�
C���ڢ�
D��ȫ��
�ο��𰸣�D
���������
�����Ѷȣ���