微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 等温等压下,对于相同质量的H2、D2、T2气体,下列叙述正确的是(?)
①密度之比为1:2:3? ②质子数之比为6:3:2? ③中子数之比为0:3:4 ④体积之比为6:3:2
A.①②③④
B.②③④
C.①②
D.③④
参考答案:A
本题解析:首先根据n=m/M确定这三个气体摩尔质量M之比为1:2:3,所以三者物质的量之比为6:3:2,再根据PV=nRT,其中P、T都相等,R为常数也不变,所以V与n成正比,因此体积V之比为6:3:2。再根据导出公式PM=ρRT得出ρ与M成正比,所以气体密度ρ之比为1:2:3。这三种气体由于都是氢原子组成的双原子分子,所以当物质的量相同时其质子数相同时1:1:1,那么物质的量之比为6:3:2,所以质子数之比为6:3:2。三个气体中中子数分别为0、2、4,因此在与物质的量相乘得到中子数之比为0:3:4。
本题难度:一般
2、选择题 在相同的温度和压强下,二氧化碳和笑气(化学式为N2O)的体积相同,则下列它们的( ?)一定相同。
(1)分子数 (2)原子数 (3)密度 (4)质量 (5)物质的量
A.只有(1)(5)
B.只有(1)(2)(4)(5)
C.只有(2)(3)(4)(5)
D.(1)(2)(3)(4)(5)
参考答案:D
本题解析:根据阿伏加德罗定律以及推论可知,在相同条件下,相同体积的任何气体具有相同的分子数,也具有相同的额占到了。又因为二者都是由3个原子构成的,且二者的相对分子质量相等,所以它们的原子数和质量也是相等。同样在相同条件下,气体的密度之比是相应的摩尔质量之比,所以密度也是相等的,答案选D。
点评:该题是高考中的常见考点,属于中等难度的试题,试题基础性强,侧重对学生灵活运用阿伏加德罗定律解决实际问题的能力,有利于培养学生的逻辑推理能力。该题的关键是记住阿伏加德罗定律的具体内容,特别是使用范围和注意事项。
本题难度:简单
3、填空题 同温同压下,等质量的SO2和NO2的密度之比为______.
参考答案:设气体的质量都为1g,则二者的物质的量之比为1g64g/mol:1g46g/moL=23:32,
同温同压下,气体的物质的量之比等于体积之比,
所以等质量的SO2和NO2的密度之比为1g23L:1g32L=32:23,
故答案为:32:23.
本题解析:
本题难度:一般
4、选择题 由H79Br和H81Br组成的混合气体对N2的相对密度为2.9,则气体中79Br和81Br的原子个数比为( )
A.1:1
B.1:2
C.2:3
D.3:2
参考答案:根据ρ=MVm知,相同条件下,两种气体的密度之比等于其相对分子质量之比,所以H79Br和H81Br组成的混合气体的平均摩尔质量为81.2,则79Br和81Br的平均相对原子质量为80.2,
,
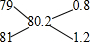
79Br和81Br物质的量之比为0.8:1.2=2:3,其原子个数之比为2:3,故选C.
本题解析:
本题难度:简单
5、选择题 同温同压下,相同体积的CO2、CO、H2、O2,质量按从大到小的顺序排列正确的是(?)
A.H2>O2>CO>CO2
B.CO2>O2>CO>H2
C.H2>CO>O2>CO2
D.CO2>H2>O2>CO
参考答案:B
本题解析:根据阿伏加德罗定律可知,在相同条件下,相同体积的任何气体含有相同数目的分子,因此气体的物质的量也是相同的。所以根据m=n・M可知,气体的相对分子质量越大,气体的质量就越大,所以正确的答案选B。
本题难度:一般