��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� 50 mL 0��50 mol��L��1������50 mL 0��55 mol��L��1NaOH��Һ��ͼʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
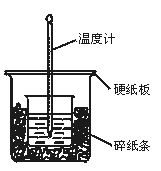
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��?��
��2���ձ���������ֽ����������?��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ?���ƫ��ƫС������Ӱ�족����
��4��ʵ���и���60 mL 0��50 mol��L��1�����50 mL 0��55 mol��L��1NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������?�����ȡ�������ȡ����������к���?�����ȡ�������ȡ������������ɣ�?��
2��ѡ���� ��֪Zn(s)+H2SO4(aq)= ZnSO4(aq)+H2(g) ��H <0�����й��ڸ÷�Ӧ�������в���ȷ����?
[? ]
A���÷�Ӧ�оɼ������������������¼��γ���ų���������������������
B�������Ȼ�ѧ����ʽ�С�H��ֵ�뷴Ӧ���������
C���÷�Ӧ�Ļ�ѧ�ܿ���ת��Ϊ����
D���÷�Ӧ��ѭ�����غ㼰��ʧ�����غ�
3��ѡ���� �����й�������˵������ȷ���� ��������
A����ʯ��Դ�����ڲ������Ŵ���������
B��ֲ��Ĺ������ʹ̫����ת��Ϊ��ѧ��
C��ȼ��ȼ��ʱֻ�ǽ���ѧ��ת��Ϊ����
D����ʯī�ƽ��ʯ�����ȷ�Ӧ����ʯī�����Ƚ��ʯ������
4��ѡ���� ������H2SO4��Һ�м���100mL 0.4 mol��L��1Ba(OH)2��Һ���ų���������5.12 kJ�����������Ba(OH)2��Һ�м���100mL 0.4 mol��L��1HCl��Һʱ���ų�������Ϊ2.2 kJ����Na2SO4��Һ��BaCl2��Һ��Ӧ���Ȼ�ѧ����ʽΪ? (����)
A��Ba2��(aq)��SO42��(aq)=BaSO4(s)����H����2.92 kJ��mol��1
B��Ba2��(aq)��SO42��(aq)= BaSO4(s)����H����18 kJ��mol��1
C��Ba2��(aq)��SO42��(aq)=BaSO4(s)����H����73 kJ��mol��1
D��Ba2��(aq)��SO42��(aq)=BaSO4(s)����H����0.72 kJ��mol��1
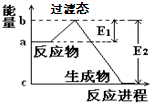
5������� ��1��20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ�����Ƿ�ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ��______������ȡ����ȡ�����Ӧ��NO2��CO��������______�����������������=����CO2��NO����������
��2����ij���Ϊ2L���ܱ������г���1.5mol?NO2��2mol?CO����һ�������·�����Ӧ��NO2+CO�TCO2+NO��2minʱ�����������NO�����ʵ���Ϊ0.5mol����
�ٸö�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ����Ϊ______��12minʱ������������������ʵ���Ϊ______��
�ۼ���˷�Ӧ��5minʱ�ﵽƽ�⣬���ʱ����������������ʵ���______������ڡ�����С�ڡ����ڡ���2minʱ����������������ʵ�����