微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体。X、Y、Z是化合物,X溶液呈淡绿色,Y、Z的溶液都能使KSCN溶液变红。它们之间有如下图所示转化关系。
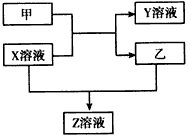
请回答:
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,此液体不具有的性质是___________。
A. 光束通过该液体时形成光亮的“通路”
B. 插入电极通过直流电后,有一极附近液体颜色加深
C. 向该液体中加入硝酸银溶液,无沉淀产生
D. 将该液体加热蒸干、灼烧后,有氧化物生成
(2)①单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为_________________(用化学式表示)。
②少量单质甲通入X溶液中发生的离子方程式为_____________。
(3)实验室制备、收集纯净干燥的甲单质,所需仪器如下,装置A为发生装置;除装置A中所需的药品外,其他装置中供选择的药品有:浓硫酸、碱石灰、五氧化二磷、饱和食盐水、氢氧化钠溶液。
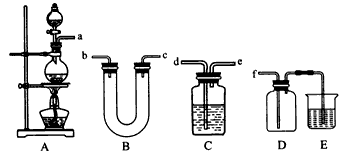
①装置A中发生反应的化学反应方程式:_____________。
②按气流的方向连接各仪器接口,顺序为 a→____→____→____→____→f
③指出装置B、C、E中的药品(从提供的药品中选择):B_______, C:_______,E:________。
参考答案:(1)C
(2)①Cl2>Br2>Fe3+;②Cl2+2Fe2+=2Cl-+2Fe3+
(3)①MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;②a→d→e→b或(c)→c或(b)→f;③B:五氧化二磷;C:饱和食盐水;E:氢氧化钠溶液
MnCl2+Cl2↑+2H2O;②a→d→e→b或(c)→c或(b)→f;③B:五氧化二磷;C:饱和食盐水;E:氢氧化钠溶液
本题解析:
本题难度:一般
2、实验题
研究性学习小组进行SO2的制备及性质探究实验。
(1)根据反应Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O,制备SO2气体。①用下列简图,画出制各并收集SO2的实验装置(含试剂)示意图。
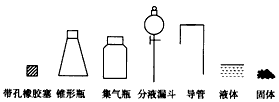
②实验过程中,使用分液漏斗滴加浓硫酸的操作是_______________________ 。
(2)将SO2气体分别通入下列溶液中:①品红溶液,现象是__________________。②溴水溶液,现象是__________________。③硫化钠溶液,现象是__________________________。
(3)有一小组在实验中发现SO2产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满):
①原因______________,验证方法__________________________;
②原因______________,验证方法__________________________;
③原因______________,验证方法__________________________。
参考答案:(1)①
②打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加
(2)①溶液褪色②溶液褪色③有浅黄色沉淀生成(或溶液变浑浊)
(3)①Na2SO3变质;取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液,有白色沉淀生成,则证明该Na2SO3固体变质
②不是浓硫酸;用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸
本题解析:
本题难度:一般
3、实验题 实验室用如图装置来制备乙炔,并验证乙炔的某些化学性质,制备的乙炔气体中往往含有少量的H2S气体,请按下列要求填空:
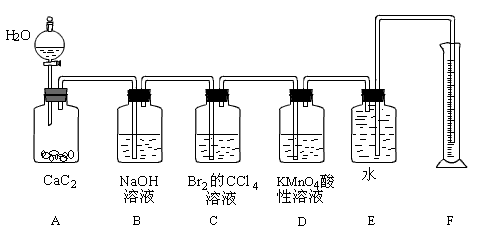
(1)实验室制乙炔反应的化学方程式是__________;为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用__________来代替水。
(2)装置B中盛放有足量的NaOH溶液的作用是_________,反应的离子方程式是___________。
(3)装置C中观察到的现象是__________,反应的方程式是__________,该反应的类型是_________。
(4)装置D中观察到的现象是_________,该反应的类型是____________。
参考答案:(1)CaC2+2H2O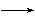 Ca(OH)2+ CH
Ca(OH)2+ CH 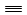 C H ( 或C2H2)↑;饱和食盐水
C H ( 或C2H2)↑;饱和食盐水
(2)除去H2S,否则H2S也能与Br2的CCl4溶液、酸性KMnO4溶液反应 ;H2S +2OH-==S2-+2H2O
(3)溴的颜色(橙红色)逐渐褪去;
CH 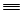 CH+Br2
CH+Br2 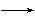 CHBr=CHBr或CH
CHBr=CHBr或CH 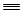 CH+2Br2
CH+2Br2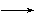 CHBr2CHBr2 ;加成反应
CHBr2CHBr2 ;加成反应
(4)紫色逐渐褪去;氧化反应。
本题解析:
本题难度:困难
4、实验题 氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。
(1)工业上通常采用电解法制氯气,其反应原理为:(用化学方程式表示)_____________________。某化学兴趣小组欲采用图一装置制取氯气,并探究氯气的性质。

指出图一装置中的错误之处_____________、____________,
(2)丙装置的作用_____________。丙装置中发生反应的离子方程式______________________。
(3)为了制得干燥纯净的Cl2,请你结合图二将以上装置重新排序:_____________。
(4)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是_____________。
A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3
(5)为证明氯气的强氧化性,有同学将图一中的“乙”换成“己”,你认为他这样做对吗?_____________。为什么?__________________________。
参考答案:(1)反应原理为:2NaCl+2H2O 2NaOH+H2↑+Cl2↑;未用石棉网;用长颈漏斗而未用分液漏斗
2NaOH+H2↑+Cl2↑;未用石棉网;用长颈漏斗而未用分液漏斗
(2)吸收多余氯气,防止环境污染;Cl2+2OH-=Cl-+ClO-+H2O
(3)甲 戊 丁 乙 丙
(4)AC
(5)不对;使石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
本题解析:
本题难度:一般
5、选择题 下图是实验室制取氨气的装置和选用的试剂,其中正确的是
A. 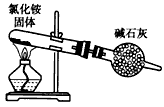
B. 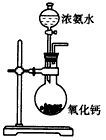
C. 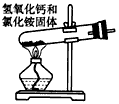
D. 
参考答案:BD
本题解析:
试题分析:
A 、NH4Cl 固体受热分解生成NH3 和HCl ,而当温度降低时,NH3 和HCl 又重新化合成固体NH4Cl ,气体进入干燥管的机会不多,故A 错误;
B 、向CaO 中滴加浓氨水,CaO 遇水生成Ca (OH )2 ,同时放出大量热量,使浓氨水中的氨气逸出,故B 正确;
C 、固体加热制气体时,试管口应略向下倾斜,使产生的水能够流出,以免损坏试管,故C 错误;
D 、浓氨水易挥发,浓氨水加热制取NH3 的方法和试剂都是正确的,故D 正确.
故选BD
本题难度:一般