��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��ij��Һ����μ���NaOH��Һʱ��������ɳ�����������������NaOH������仯��ͼ��ʾ�������Һ�д������е����ӿ�����
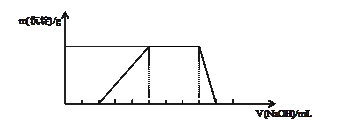
A��H+��NH4+��Al3+��NO3-
B��H+��Al3+��AlO2-��SO42-
C��H+��NH4+��Mg2+��Cl-
D��NH4+��Al3+��Cl-��SO42-
�ο��𰸣�A
�������������ͼ���֪����ʼ������������˵����Һ�к��������ӣ����������ʱ�����������������ƣ��������仯�������ճ�����ʧ�������ɳ������ܽ�������ĵ�����������3�U1�ģ�����һ�����������ӣ�����ѡ��A��ȷ��CD����ȷ��B�����Ӳ��ܴ������棬��ѡA��
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ����2H++S2-��H2S������ʾ����
A.Na2S��Һ�����ᷴӦ
B.FeS��ϡ���ᷴӦ
C.K2SͶ��ŨH2SO4��
D.K2S�������ᷴӦ
�ο��𰸣�A
���������
�����Ѷȣ���
3��ѡ���� ��֪X��M������ѧ�̲ij���Ԫ�أ����жԼס����������ӷ�Ӧͨʽ���ƶ��У����ף�XO3n��+Xn��+H����X����+H2O��δ��ƽ�������ң�Mm��+mOH����M(OH)m����������ȷ���ǣ�?��
����n=1����XO3n����XԪ��Ϊ+5�ۣ�Xλ�����ڱ��ڢ�A��
����m=1����M(NO3)m��Һ�Ͱ�ˮ����ʱ��������ܲ�ͬ
����m=2�����ڿ���������MSO4��Һ������һ���ܵõ�MSO4
����n=2����X����������ˮ��������������⻯�ﷴӦ
����m=3����MCl3�������ļ���Һ��Ӧһ������M(OH)m
����n=2��m=3����Xn����Mm�������ķ�Ӧ��ˮ�ⷴӦ
A���٢�
B���ڢ�
C���٢ڢۢ�
D���������
�ο��𰸣�B
�������������n=1����X����ͼ�Ϊ-1�ۣ�XӦλ�����ڱ��ĵ�VIIA�壬������m=1�� +1���������У�Ag+��Na+��K+�ȣ�ֻ������������������ˮ�ij�����Ag++OH-=AgOH���������������ڰ�ˮ����������Һ���백ˮ������������Һ������������ˮ������������Һ�� ���������������μӳ����ܽ⣬����˳��ͬ����ͬ����ȷ����m=2����MΪFe������������+2�����ڿ������ױ�����Ϊ+3�ۣ�����������Һ�����ɡ����ղ����ܴﵽ��������������n=2��XԪ���γ�X2-���ӣ�X��ͼ�Ϊ-2�� Xֻ��Ϊ��������⣬Ũ���Ậ��ǿ�����ԣ������������⣬��ȷ����m=3������������ֻ�������������������Ȼ��������������Ʒ�Ӧ����û�����������������ɣ�������n=2��m=3��Xn-��Mm+���Էֱ���S2-��Fe3+�����߷���������ԭ��Ӧ���������Դ�ѡB��
�����Ѷȣ�һ��
4��ѡ���� ���и�����������ָ�������д����������
A.��C(HCO3-)=0.1mol/L����Һ��NH4+��Al3+��Cl-��NO3-
B.����ˮ�������C(H+)=1��10-12mol/L����Һ��AlO2-��HCO3-��Na+��SO42-
C.��ʹ��ɫʯ����ֽ��������Һ��SO32-��CO32-��Na+��K+
D.PH=1����Һ��Mg2+��Fe2+��NO3-��[Ag(NH3)2]+
�ο��𰸣�C
������������������A��HCO3-�� NH4+��Al3+�ܷ���˫ˮ�ⲻ�ܴ������档�ʴ�
B����ˮ�����c��H+��=10-12mol?L-1����Һ��ˮ�ĵ����ܵ����ƣ�����Ϊ�������Һ��HCO3-�������ᷴӦ������Ӧ��AlO2-�����ᷴӦ����������һ�����ܴ������棬�ʴ���
C����������ʹ��ɫʯ����ֽ������SO32-��CO32-��Na+��K+�����ڼ�����Һ�й��档
D��PH=1����Һ�����ԣ�NO3-�������о��������Խ�Fe2+���������������ӣ��ʴ�
���㣺���ӹ�������
���������⿼�����ӵĹ������⣬��ȷ������Ϣ���ھ��Ӧ���ǽ��Ĺؼ�������Ϥ���Ӳ��ܹ���ij�����ԭ�ɽ��
�����Ѷȣ���
5��ѡ���� �����£����и���������ָ����Һ��һ���ܴ����������
A.0.1mol?L-1?Na2CO3��Һ��
B.0.1mol?L
C.0.1mol?L-1 FeCl3��Һ��
D.=1��1014����Һ����
�ο��𰸣�D
���������������A������֮��������̼�ᱵ������
B��OH-��HCO3-��Ӧ��
C��Fe3+��I-����������ԭ��Ӧ��
D.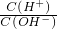 =1��1014����Һ��c��H+��=1mol/L����Һ�����ԣ�
=1��1014����Һ��c��H+��=1mol/L����Һ�����ԣ�
���A����Ba2+��CO32-����֮��������̼�ᱵ���������ܹ��棬��A����
B����OH-��HCO3-��Ӧ����ˮ��̼������ӣ����ܹ��棬��B����
C��Fe3+��I-����������ԭ��Ӧ�����ܹ��棬��C����
D.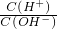 =1��1014����Һ��c��H+��=1mol/L����Һ�����ԣ���������֮�䲻��Ӧ���ܹ��棬��D��ȷ��
=1��1014����Һ��c��H+��=1mol/L����Һ�����ԣ���������֮�䲻��Ӧ���ܹ��棬��D��ȷ��
��ѡD��
���������⿼�����ӵĹ��棬��ȷ���ֽⷴӦ����������������֮��ķ�Ӧ���ɽ����Ŀ�ѶȲ���
�����Ѷȣ���